
I) les Astrocytes :
1) Cytophysiologie générale :
Au sein du SNC, les cellules de la névroglie sont deux fois plus nombreuses que les neurones et sont majoritairement astrocytaires (dessin Ramon y Cajal, 1907) Les astrocytes sont de petites cellules étoilées dont le corps cellulaire à un diamètre d'environ 10 microns et dont les prolongements cellulaires s'étendent de façon radiée. Au plan ultrastructural, les astrocytes présentent 3 principales caractéristiques :
* la présence de filaments intermédiaires particuliers, les gliofilaments. Ces filaments intermédiaires sont groupés en faisceaux et sont composés d'une protéine spécifique des astrocytes : la GFAP, "glial fibrillary acidic protéin" ou protéine acide gliofibrillaire.
* la présence de grains de glycogène , absent des autres cellules nerveuses, disséminées dans le corps cellulaire, les prolongements cytoplasmique et plus particulièrement au niveau des extrémités distales de ces prolongements : les pieds astrocytaires.
* la présence de jonctions interastrocytaires de type "gap" qui permettent la signalisation intercellulaire via des canaux jonctionnels constitués de molécules de connexine 43. Ces jonctions sont le support anatomique de réseaux fonctionnels astrocytaires qui viennent se superposer aux réseaux neuronaux.
2) Classification :
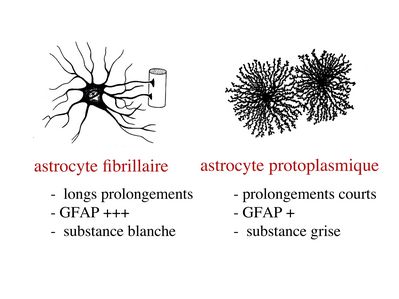
a) classification morphologique : on distingue 2 principales catégories d'astrocytes :
- les astrocytes fibrillaires (ou fibreux) présentent de longs prolongements radiaires, sont riches en gliofilaments et sont localisés préférentiellement au niveau de la substance blanche (i.e zones riches en axones myélinisés).
- les astrocytes protoplasmiques présentent des prolongements courts, contiennent peu de gliofilaments, et sont localisés préférentiellement au niveau de la substance grise ( zones riches en corps cellulaires neuronaux).
Ce sont les principales morphologies adoptées par les astrocytes mais des sous-populations astrocytaires spécifiques de certaines régions du SNC peuvent adopter d'autres morphologie. Un exemple est donné par les différents types morphologiques d'astrocytes observés dans le cervelet (planche ci-dessous):
b) classification fonctionnelle : elle ne recoupe pas la classification morphologique. On distingue :
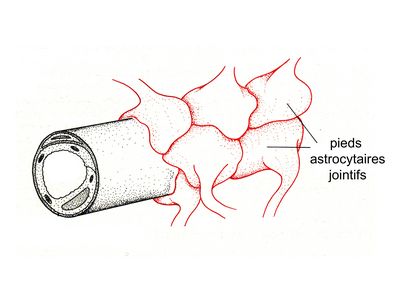
- les astrocytes de type 1: ils jouent un rôle de barrière et leurs pieds astrocytaires établissent des contacts soit avec la paroi des capillaires (participent à la barrière hémato-tissulaire, planche ci-dessous) , soit avec les méninges ( participent à la glia limitans).
- les astrocytes de type 2 jouent un rôle de soutien métabolique et trophique vis-à-vis des neurones et des oligodendrocytes. Leurs pieds astrocytaires établissent des contacts soit avec la synapse, soit avec l'axone, soit au niveau du corps cellulaire neuronal.
3) Fonctions :
a) fonction de barrière : les astrocytes de type 1 participent à la constitution de deux barrières physiques nécesssaires à la protection du tissu nerveux.
* au niveau de la barrière hémato-tissulaire entre sang et parenchyme nerveux, les pieds astrocytaires reposant sur la membrane basale des capillaires sont jointifs, et sopposent à la pénétration de cellules et de molécules sanguines.
* au niveau de la barrière entre liquie céphalorachidien (LCR) et parenchyme nerveux, les prolongements astrocytaires reposent sur la lame basale de la tunique interne des méninges (la pie-mère) et constituent la glia limitans.
b) fonctions métaboliques :
* apport énergétique : les astrocytes captent le glucose présent dans le liquide interstitiel du SNC en particulier au pourtour des micrvaisseaux et sont capables de le stocker sous forme de glycogène. En fonction des besoins métaboliques des neurones et des oligodendrocytes, les astrocytes catabolise le glycogène et fournissentt un apport énergétique sous forme de lactate.
* maintien de lhoméostasie ionique : la régulation de la concentration ionique et du volume extracellulaire au sein du tissu nerveux est essentiellement assurée par les astrocytes via des pompes et des transporteurs ioniques gliaux.
* régulation de la transmission synaptique : cette régulation est réalisée par recapture de neurotransmetteurs au niveau de la fente synaptique. Cette recapture concerne notamment du glutamate et s'effectue par des transporteurs spécifiques.
c) fonctions trophiques : s'ajoutant à leurs fonctions purement métaboliques, les astrocytes synthétisent un ensemble de molécules solubles ou membranaires qui conditionnent la survie et la plasticité des cellules environnantes. Parmi ces molécules, citons la famille des neurotrophines à laquelle appartient le NGF (« Nerve Growth Factor »). On sait également que les astrocytes jouent un rôle important dans l'induction de la synaptogénèse (développement et plasticité) via des molécules qui ne sont pas identifiées.
d) fonctions immulogiques : si les cellules microgliales sont les seules cellules du SNC dérivant du système immunitaire, les astrocytes bien que dérivant de cellules souches neurales exercent un certain nombre de fonctions immunitaires en situation inflammatoire. Parmi celles-çi, citons 2 fonctions essentielles :
* la synthèse de cytokines :
pour mémoire, cytokines pro-inflammatoires (IL-1, IL-6, TNF) ou anti-inflammatoires (TGF-beta)
* la présentation d'antigène aux lymphocytes T : les astrocytes sont après les cellules microgliales, les principales cellules présentatrices d'antigène au sein du parenchyme nerveux.
4) Les réseaux astrocytaires
a) généralités : Les astrocytes établissent des connexions intercellulaires de type jonctions "gap" qui permettent le passage d'ions et de molécules au sein de réseaux astrocytaires. Ces réseaux forment de véritables syncitium fonctionnels ou s'échangent et se propagent les molécules et les ions notamment les ions calcium. Ces zones d'échange peuvent ainsi s'étendre jusqu'à 300 micron au delà d'une cellule et englober le cytoplasme de plusieurs dizaines de cellules. Les connexons formant les canaux jonctionnels interastrocytaires sont exclusivement constitués de connexine 43 (pour mémoire : il existe environ 12 types de connexine codées par 2 familles géniques distinctes. Toutefois la connexine 43 n'est pas spécifiquement astrocytaire mais également synthétisée par d'autre types cellulaires à l'extérieur du SNC : cardiomyocytes par exemple). Le niveau d''expression astrocytaire de la connexine 43 et donc l'importance du couplage interastrocytaire varient in vivo en fonction de la région et de l'état de maturation du SNC. Elle peut être également fortement augmenté au cours de certaines situations pathologiques.
b) fonctions :
* homéostasie métabolique : bien que non formellement prouvé, il est admis que les réseaux astrocytaires forment des zones tampons permettant de dissiper toute modification métabolique locale. La régulation de la concentration ionique et du volume extracellulaire au sein du tissu nerveux est ainsi maintenue à léchelle de lastrocyte et des réseaux astrocytaires. Par ailleurs, la fonction astrocytaire de recapture des neurotransmetteurs au niveau de la fente synaptique est également facilitée par les réseaux astrocytaires qui limitent laccumulation locale de neurotransmetteurs au sein des astrocytes péri-synaptiques.
* transfert de signaux informatifs : à limage des synapses pour les réseaux neuronaux, les jonctions inter-astrocytaires pourraient permettrent la circulation dinformations qui coordonnent lactivité astrocytaire. Ainsi, on considère actuellement que lactivité et le niveau dexcitabilité des réseaux neuronaux est contrôlée par les réseaux astrocytaires de voisinage. Au sein des réseaux astrocytaires, le substratum de linformation nest pas londe de dépolarisation mais essentiellement la concentration intracytosolique de calcium. Différents types de stimulis appliqués localement au niveau dun astrocyte peuvent ainsi provoquer des vagues calciques. Ces vagues se propagent aux astrocytes voisins et modifient de façon coordonnée lactivité de toute une série de messagers intracellulaires.
II) La myéline du système nerveux central
1) Les oligodendrocytes : on distingue deux types doligodendrocytes. Les oligodendrocytes myelinisants, encore appelés oligodendrocytes interfasciculaires, forment la gaine de myéline entourant la plupart des axones du système nerveux central. Les oligodendrocytes non myélinisants, encore appelés oligodendrocytes satellites, sont localisés à proximité des corps cellulaires neuronaux. Nous naborderons ici que les oligodendrocytes myélinisants. En microscopie électronique, les oligodendrocytes myélinisants ont un corps cellulaire petit, de 6 à 8 microns de diamètre, rond, avec un cytoplasme foncé quie ne contient pas de gliofilament (à la différence des astrocytes). Chaque oligodendrocyte envoie des prolongements de sa membrane plasmique s'enroulant autour de plusieurs axones adjacents.
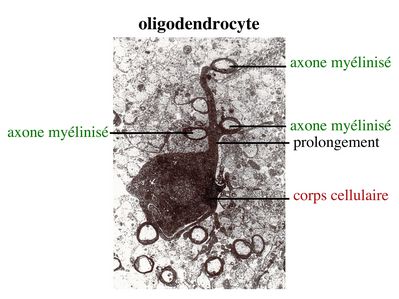
2) formation et ultrastructure : la gaine de myéline est constituée par lenroulement compact, en spirale, de la membrane plasmique des oligodendrocytes. Cette gaine de myéline recouvre les axones par segments courts de 1mm de long, interrompus par des espaces non myélinisés, appelés noeuds de Ranvier.
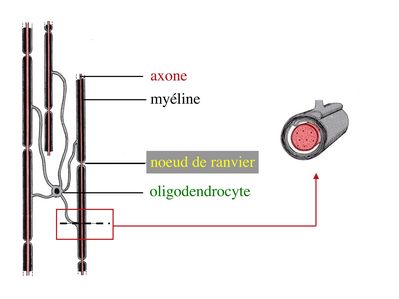
Au niveau des noeuds de Ranvier, longs de quelques microns, laxone est dénudé, présente un renflement de son cytoplasme et exprime un certain nombre de molécules spécifiques, notamment des canaux sodium.
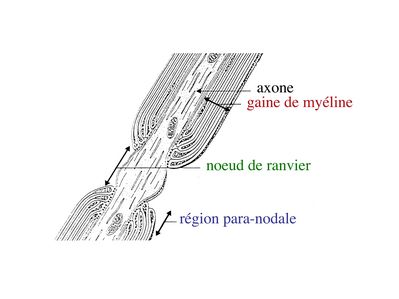
Par ailleurs, on observe au niveau du noeud de Ranvier la présence de pieds astrocytaires (astrocytes de type 2) faisant contact avec la membrane plasmique axonale. À proximité des noeuds de Ranvier, la gaine de myéline sinterrompt de manière échelonnée le long de laxone, en délimitant la région paranodale .
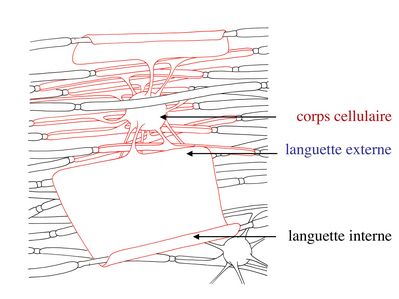
Au cours du développement, le prolongement dun oligodendrocyte doit senrouler environ 40 fois autour de laxone pour former la gaine de myéline. Dans cet enroulement de membrane plasmique, la partie la plus interne, au contact de laxone, est appelée languette interne. La partie la plus externe de lenroulement est appelée languette externe.
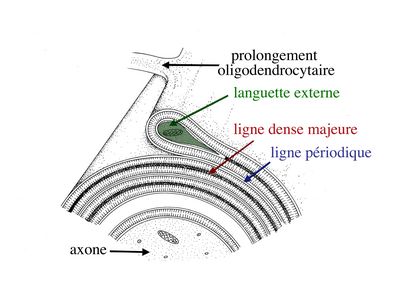
Dans la partie enroulée et compactée de la gaine de myéline, le cytoplasme oligodendrocytaire, localisé entre les feuillets internes de la membrane plasmique, disparaît complètement. Ainsi, les feuillets internes saccolent et forment la ligne dense majeure. Les feuillets externes de la membrane plasmique oligodendrocytaire saccolent également, mais en laissant persister un espace extracellulaire qui va constituer la ligne claire ou ligne périodique.
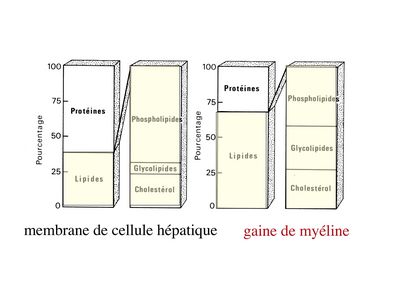
3) composition biochimique : à la différence de la membrane plasmique de la très grande majorité des cellules de l'organisme, la membrane plasmique constituant la gaine de myéline est composée à 70% de lipides. Parmi ceux-ci, certains sont caractéristiques de la myéline tels que le galactocéramide (ou galactosyl-céramide). La fraction protéique de la gaine de myéline comprend un certain nombre de molécules spécifiques tel que la protéine basique de la myéline (MBP pour "myelin basic protein"), la MOG ("myelin oligodendrocyte glycoprotein") et la MAG ("myelin associated glycoprotein") (la MAG est une protéine minoritaire de la myéline centrale alors qu'elle est majoritaire dans la myéline périphérique).
4) fonctions : du fait de sa forte teneur en lipides, la gaine de myéline est imperméable aux éléments hydrophiles constitue donc un bon "isolant électrique" entre le milieu intracellulaire, c'est-à dire le cytoplamse axonal, et le milieu extracellulaire. En facilitant la conduction de linflux nerveux au niveau des segments myélinisés de laxone, la gaine de myéline détermine le caractère saltatoire de la conduction nerveuse c'est-à-dire une conduction par sauts rapides dun noeud de Ranvier à un autre. Les fibres myélinisées dont les axones sont les plus larges ont les gaines de myéline les plus épaisses (donc le plus grand nombre de tours de spire), les internodes les plus longs (internode = distance entre 2 noeuds de Ranviers consécutifs) et la vitesse de conduction la plus élevée.
5) pathologie : chez l'adulte jeune, la pathologie la plus fréquente de la myéline du système nerveux central est la sclérose en plaques. Il s'agit d'une maladie auto-immune au cours de laquelle les antigènes cible sont les protéines de la myéline du système nerveux central, et enparticulier la MBP et la MOG. On observe la présence de multiples zones de démyélinisation, disséminées dans le système nerveux central et le plus souvent accompagnées d'une infiltration lymphocytaire et macrophagique. Au plan clinique, la sclérose en plaques se caractérise le plus souvent par la survenue d'épisodes transitoires de déficit sensitifs, moteurs ou sensoriels. Ces épisodes transitoires laissent parfois des séquelles qui, au fil du temps, peuvent conduire à un handicap majeur.
III) la myéline du système nerveux périphérique :
1) cellules de Schwann : à la différence des oligodendrocytes qui peuvent myélinisés plusieurs axones, une cellule de Schwann ne myélinise quun axone. Chaque cellule de Schwann forme une gaine de myéline sur un segment limité d'un axone.
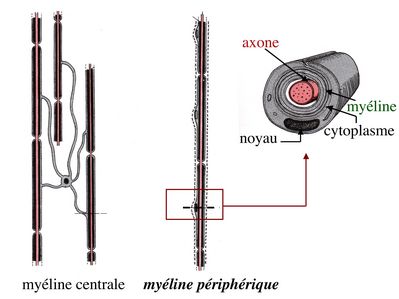
Les axones périphériques myélinisés sont ainsi associés à un ensemble de cellules de Schwann reposant sur une lame basale. Il existe également des cellules de Schwann non myélinisantes qui sont associées aux axones périphériques non myélinisés ou qui sont localisés dans les ganglions végétatifs ou sensitifs.
2) formation et ultrastructure : la formation et l'ultrastructure de la myéline périphérique sont similaires à celles de la myéline centrale.
3) composition biochimique : la myéline périphérique ne présente pas la même composition biochimique que la myéline centrale, en particulier au niveau protéique. On retient la présence abondante de protéine P0, de MAG ("myelin associated glycoprotein") et de PLP ("peripheral lipoprotein").
4) pathologie : au cours des neuropathies à IgM avec anticorps anti-MAG, une immunoglobuline de type M synthétisée par un clône lymphocytaire B à prolifération non contrôlé reconnaît la protéine myélinique MAG. On observe alors en microscopie électronique un aspect caractéristique de myéline décompactée.
IV) la microglie :
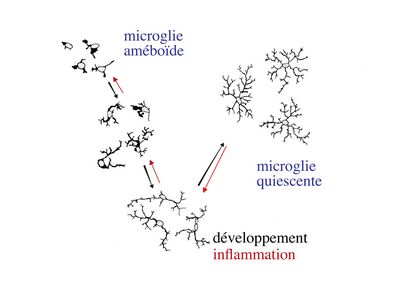
Les cellules microgliales représentent environ 5% de l'ensemble des cellules du système nerveux central. À la différence des autres cellules nerveuses qui dérivent du neurectoderme, les cellules microgliales dérivent de cellules souches hématopoïétiques (donc du mésoderme) et appartiennent au système immunitaire. La microglie constitue la population de macrophages tissulaires spécifiques du système nerveux central. La morphologie des cellules microgliales varie en fonction de leur état dactivation. Au cours du développement cérébral, la microglie est activée et présente une morphologie améboïde (ou amiboïde) car elle est globalement ovalaire avec de très courts prolongements cytoplasmiques. Elle participe alors essentiellement à lélimination des débris cellulaires amis également à lélimination ciblée de populations neuronales. Ultérieurement, au cours de la maturation du système nerveux central, la microglie activée se différencie en microglie quiescente (microglie au repos). Elle adopte progressivement une morphologie ramifiée avec un corps cellulaire qui devient petit et ovoïde. Des données récentes montrent que les ramifications de la microglie quiescente sont en mouvement constant, alors que le corps cellulaire reste fixe. On considère que ces mouvements permettent une immunosurveillance de lensemble du périmètre couvert par les ramifications microgliales. En situation inflammatoire, on observe une activation des cellules microgliales caractérisée au plan morphologique par une rétraction des ramifications et une hypertrophie du corps cellulaire. Au plan fonctionnel, cette activation saccompagne dune augmentation de la capacité de phagocytose, de lexpression de molécules dhistocompatibilité classe II et de la synthèse de cytokines pro-inflammatoires.
V) les épendymocytes :
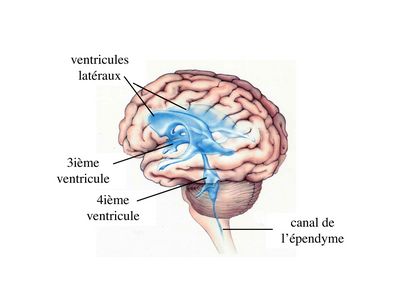
1) cytophysiologie générale : les épendymocytes tapissent la paroi de cavités localisées au coeur du tissu nerveux qui sont les cavités ventriculaires au niveau du cerveau et le canal de lépendyme au niveau de la moelle épinière. Ces cavités sont remplies dun liquide paucicellulaire (contenant peu de cellules) dans lequel baigne lensemble du système nerveux central: le liquide cépahlorachidien (LCR).
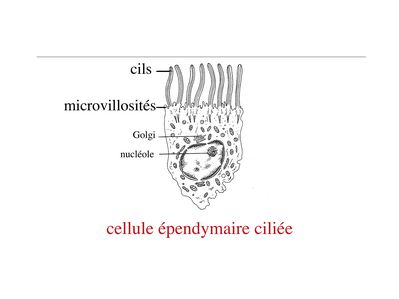
Les cellules épendymaires sont des cellules polarisées présentant un pôle apical en contact avec le LCR. On observe, au niveau du domaine apical, une différenciation de la membrane plasmique sous forme de cils et/ou de microvillosités. Par ailleurs, les cellules épendymaires sont réunies par des jonctions gap. Il existe deux types de cellules ependymaires : les cellules épendymaires ciliées et les tanicytes.
2) les cellules épendymaires ciliées : elles présentent de nombreux cils et microvillosités se projetant au contact du LCR et dont le rôle est de faciliter la circulation du LCR.
3) les tanicytes : leur surface apicale présente uniquement des microvillosités alors que sur leur versant basal, ils envoient de longs prolongements. Ceux-ci établissent des contacts, dans le parenchyme nerveux, avec des capillaires sanguins, des neurones et des astrocytes.
4) rôle des épendymocytes : outre leur fonction dans la circulation du LCR, les cellules épendymaires et notamment les tanicytes participent aux échanges LCR/parencyme via labsorption coté apical puis la sécrétion coté basal dhormones, de neuromédiateurs ou dautres molécules contenues dans le LCR. Une autre fonction des cellules épendymaires est de former une niche pour les cellules souches neurales localisées dans la couche dite sous-épendymaire bordant la paroi des ventricules cérébraux.
VI) la barrière hémato-encéphalique :
Lune des principales caractéristiques du SNC est dêtre inaccessible à un grand nombre de molécules sanguines qui pénètrent pourtant librement, ou de façon faiblement restreinte, dans la plupart des autres tissus de lorganisme. De la même façon, la circulation des cellules immunes depuis le sang vers le système nerveux central est très limitée alors que l'immunosurveillance des autres tissus de l'organisme est assurée grâce au trafic tissulaire de cellules immunes sanguines. Cette propriété du système nerveux central est due à la présence dune barrière dite "hémato-encéphalique", terme qui désigne lensemble des mécanismes qui restreignent les échanges entre dune part le sang et dautre part le LCR et le parenchyme nerveux. Ainsi, la barrière hémato-encéphalique regroupe trois interfaces ou barrières.
1) la barrière hémato-tissulaire (interface sang/parenchyme cérébral) : elle intéresse les échanges qui se font directement entre le sang et le parenchyme cérébral au niveau des capillaires sanguins.
a) structure des capillaires "cérébraux" (capillaires du système nerveux central) : les capillaires cérébraux sont formés dune monocouche de cellules endothéliales reposant sur une membrane basale continue qui se dédouble par endroits pour accueillir des péricytes (cellules musculaires lisses assurant la contractilité des microvaisseaux, présentes dans tous les capillaires de l'organisme et ayant une double valence musculaire et immune, Cf cours Epithélium N°2) et des macrophages dénommés macrophages périvasculaires (les macrophages périvasculaires forment une population distincte des péricytes et qui est spécifique des capillaires cérébraux).
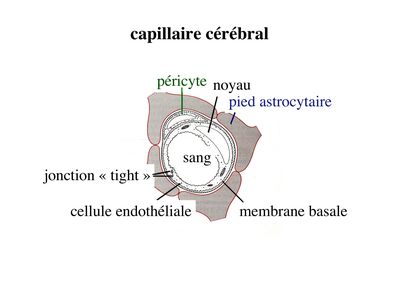
Cet endothélium se différencie des autres capillaires de lorganisme par un ensemble de caractéristiques dont les principales sont :
- la présence de jonctions serrées réunissant les cellules endothéliales. Ces jonctions serrées sont de type Zonula Occludens
- la rareté des vésicules endothéliales
- la présence d'un équipement enzymatique riche et parfois spécifique
- l'absence de tissu conjonctif périvasculaire içi remplacé par les prolongements astrocytaires des astrocytes de type 1.
- l'existence de macrophages périvasculaires localisés dans un dédoublement de la lame basale.
b) fonctions :
*contrôle du passage des molécules : les macromolécules ne franchissent pas la barrièrela hématotissulaire et, pour les petites molécules, la perméabilité est identique à celle dune membrane cellulaire. On observe donc le passage libre des molécules lipophiles et la nécessité de transporteurs membranaires, parfois spécifiques, pour les molécules hydrophiles.
* contrôle du passage des cellules : à létat physiologique, le franchissement des capillaires cérébraux par des cellules sanguines est essentiellement réduit au renouvellement lent mais constant des cellules microgliales par des précurseurs dérivant de la moelle osseuse.
c) pathologie : il faut distinguer les situations de lésion de la barrière hématotissulaire des situations d'altération fonctionnelle de cette barrière. Ainsi, une véritable "une rupture" de la barrière hématotissulaire peut-être observée en cas de lésion directe de lendothélium par un traumatisme, une ischémie cérébrale (défaut transitoire ou définitif de l'apport sanguin d'un territoire cérébral), ou une invasion tumorale. On observe alors un oedème cérébral lié au passage de macromolécules, dion et deau. Une altération fonctionnelle sans lésion directe de la barrière est observée au cours de processus inflammatoires tel que la sclérose en plaques. On observe alors une activation de l'endothélium responsable de l'infiltration du parenchyme nerveux par des cellules immunes.
2) la barrière hémato-liquidienne : elle intéresse les échanges entre le sang et le LCR. Elle correspond morphologiquement à deux structures qui sont les plexus choroïdes et les villosités arachnoïdiennes assurant respectivement la production et la résorption du LCR.
a) les plexus choroïdes : ce sont des structures d'aspect villositaire, appendues à la paroi des ventricules cérébraux et constituées dun stroma et dun épithélium.
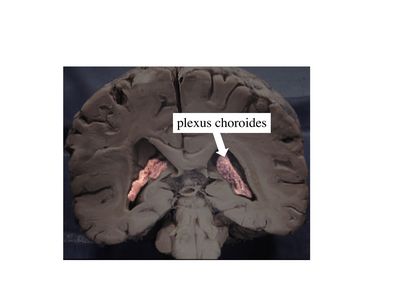
Le stroma des plexus choroïdes contient des vaisseaux qui n'ont pas la structure des capillaires cérébraux et qui laissent passer plus ou moins librement cellules et molécules.
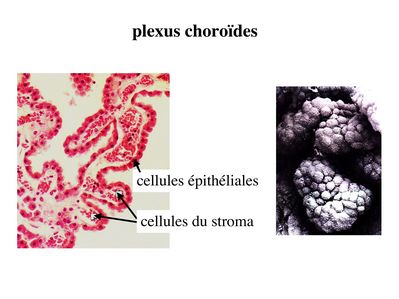
La véritable barrière est formée par l'épithélium choroidien qui recouvre le stroma. Le rôle des plexus choroides est de maintenir la composition protéique et cellulaire du LCR qui est caractérisé entre autres par la quasi-absence de cellules (liquide paucicellulaire) par par labsence de macromolécules. Les plexus choroides jouent également un rôle de filtre vis-à-vis des micro-organismes et des molécules potentiellement neuro-toxiques.
b) Les villosités arachnoïdiennes : encore appelées granulations de Pacchioni, ce sont des expansions de lespace sous-arachnoïdien faisant saillie dans la lumière du sinus veineux longitudinal supérieur lui-même localisé dans la dure-mère (tunique méningée la plus externe).
3) linterface LCR/parenchyme nerveux : les surfaces internes et externes du parenchyme nerveux sont en contact avec le LCR au niveau des interfaces épendymaires et piogliales.
a) linterface épendymaire : elle contrôle les échanges entre le LCR et le parenchyme nerveux au niveau des cavités ventriculaires et du canal de lépendyme. Les épendymocytes sont réunis par des jonctions de type gap et permettent soit un passage passif de molécules vers la matrice extra cellulaire du parenchyme soit un transport actif de molécules spécifiques qui seront essentiellement recaptées par les astrocytes et/ou les neurones.
b) linterface piogliale : cette interface est localisée entre d'une part le liquide céphalorachidien, qui circule entre les tuniques méningées externes et internes, et d'autre part la surface externe du système nerveux central. L'interface piogliale comprend une composante gliale, la glia limitans (Cf cours sur les astrocytes) et une composante méningée, la pie-mère, qui constitue la tunique méningée la plus interne.
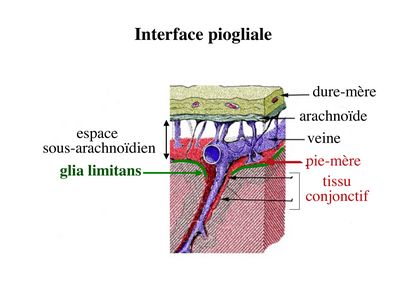
On considère que l'interface piogliale restreint faiblement les échanges entre LCR et parenchyme nerveux.
![]()