
LE TISSU EPITHELIAL
I) Notion de Tissu :
Il y a dans lorganisme 4 niveaux dorganisation cellulaire : du + simple au plus complexe : les tissus, les organes, les appareils et les systèmes. Les tissus sont des ensembles de cellules réunis par un milieu extracellulaire, la matrice extra-cellulaire. Les organes sont formés par des ensembles de tissus. Les systèmes et appareills sont constitués densembles dorganes. Chaque tissu présente des caractéristiques morphologique et fonctionnelles qui lui sont propres. 4 grandes familles de tissu regroupent la majorité des cellules de lorganisme :
- le tissu épithélial (épithélium de revêtement, épithélium glandulaire, tissus apparentés aux tissus épithéliaux i.e lendothélium, le mésothélium, les épithéliums sensoriels)
- le tissu conjonctif (TC non spécialisé ou spécialisé i.e tissu adipeux, tissu osseux, tissu cartilagineux)
- le tissu musculaire (muscle strié squelettique, muscle strié myocardique ou muscle lisse)
- le tissu nerveux (périphérique ou central).
Deux types de cellules nappartiennent pas à ces 4 catégories de tissu :
i) les populations cellulaires libres : il sagit des cellules du système hématopoïétique. Elles comprennent les cellules sanguines (globules rouges, globules blancs, plaquettes) et leur précurseurs (cellules souches, progéniteurs et précurseurs). Selon leur type et leur état de maturation, ces cellules circulent dans le sang, dans la lymphe ou dans les organes lymphoïdes (primaires : thymus, moelle osseuse rouge; ou secondaires : ganglions lymphatiques). Les cellules immunes (globules blancs) circulent également dans les tissu conjonctif et/ou dans les tissu épithéliaux.
ii) les cellules germinales : ces cellules présentent un mode de division et des particularités chromosomiques distinctes des cellules somatiques.
Les cellules participant à la composition dun tissu donné peuvent être dorigines embryologiques différentes. Par exemple, les glandes sudoripares et les glandes digestives appartiennent toutes deux au tissu épithélial glandulaire mais dérivent respectivement de lectoderme et de lendoderme. Selon le tissu, la matrice extracellulaire varie qualitativement et quantitativement. La matrice est par exemple très abondante dans le tissu conjonctif et quasiment absente dans le tissu épithélial.
Les organes correspondent au deuxième niveau dorganisation intercellulaire. On distingue les organes creux (estomac, sophage, vessie, intestin), les organes pleins (rate, foie, cerveau, pancréas). Chaque organe est composé de différents types de tissus (par exemple lintestin contient du tissu conjonctif, du tissu nerveux, du tissu musculaire et du tissu épithélial).
Les appareils forment le troisième niveau dorganisation cellulaire. Ils sont constitués densembles dorganes présentant une unité fonctionnelle. Par exemple :
- lappareil urinaire formé par le rein la vessie et les voies urinaires basses ;
- lappareil circulatoire formé par le coeur et le réseau artério-veineux,
Enfin, le terme de système est employé pour désigner un ensmble dorganes et de molécules qui présentent une unité fonctionnelle. - Le système nerveux est formé par le cerveau, la moelle épinière, les nerfs périphériques et lensemble des molécules qui participent à son fonctionnement.
- le système immunitaire (organes lymphoïdes primaires et secondaires, cellules immunes circulantes, molécules immunes)
- système endocrinien (organes endocriniens, hormones).
II) Les cellules épithéliales :
A) caractéristiques générales : le tissu épithélial « classique » (en excluant donc les tissus apparentés aux tissu épithélial) est formé de cellules dites épithéliales qui sont jointives, et reposent sur une fine lame de matrice extracellulaire nommée lame basale (ou membrane basale). Les cellules épithéliales présentent 4 principales caractéristiques:
1) la cohésion : les cellules épithéliales sont maintenues jointives par un ensemble de système de jonctions qui sétablissent entre cellules épithéliales ainsi quentre cellules épithéliales et lame basale.
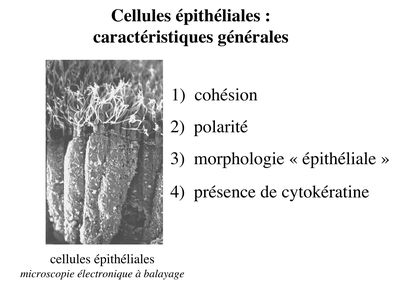
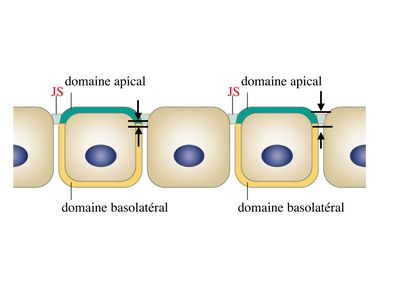
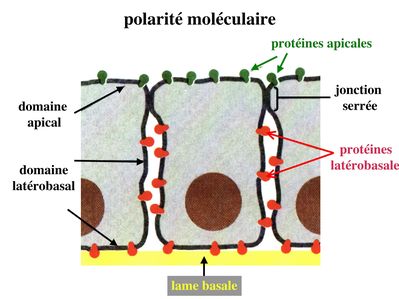
2) la polarité : les cellules épithéliales présentent une distribution très asymétrique des composants de leur cytoplasme. On parle de pôle basal pour désigner la portion de cytoplasme localisée à proximité de la lame basale et de pôle apical pour désigner le « sommet » du cytoplasme. Les cellules épithéliales présentent également une distribution asymétrique des composants de leur membrane plasmique. On distingue ainsi le le domaine basolatéral et le domaine apical.
3) la morphologie épithéliale : du fait de fortes interactions cellule-cellule et cellule-lame basale, les cellules épithéliales adoptent toujours la forme d'un cube ou d'un cylindre plus ou moins aplati (pas de forme ronde comme les cellules sanguine, étoilée comme les astrocytes et les neurones, ou fusiforme comme les cellules musculaires)
4) la présence de filaments intermédiaires de cytokératine : Les cytokératines forment une famille de 20 protéines, spécifiques des cellules épithéliales. Au sein dun même épithélium, les cellules épithéliales peuvent exprimer différents sous-types de cytokératine. Au sein dun même épithélium, on peut observer différentes sous-populations de cellules épithéliales qui expriment différentes cytokératines. Chaque type dépithélium présente un pattern dexpression des cytokératine qui lui est propre. Les cytokératines sont les filaments intermédiaires spécifiques des cellules épithéliales. On ne trouve pas dans les cellules épithéliales les filaments intérmédiares caractéristiques dautres types cellulaires : la vimentine présente dans les fibroblastes, la desmine dans les cellules musculaires, la GFAP dans les astrocytes ou encore les neurofilaments dans les neurones.
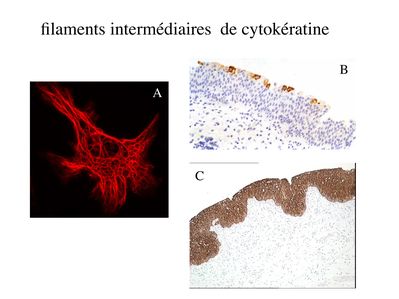
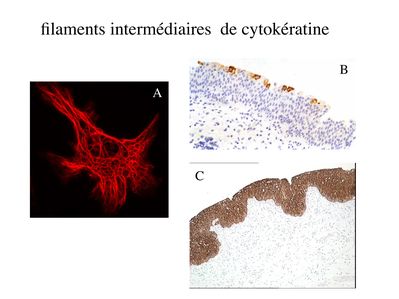
B) systèmes de jonctions :
Les systèmes de jonction assurent la cohésion et la communication au sein du tissu épithélial. Ils se divisent en 2 grandes catégories : systèmes de jonction intercellulaire et système de jonction entre cellule et lame basale.
1) Systèmes de jonction intercellulaire :
Bien quétant présents dans la plupart des tissus, ils sont particulièrement abondants dans le tissu épithélial. Aucun dentre aux nest strictement spécifique du tissu épithélial. Leur organisation au sein du tissu épithélial est par contre spécifique. On en distingue 3 types: les jonctions serrées, les jonctions dancrage et les jonctions communicantes. On parle de zonulalorsque ces systèmes de jonction (SJ) forment une ceinture ou un anneau sétendant sur une large zone de la membrane plasmique. On parle alors de macula lorsque ces SJ sétendent sur des surfaces limitées de la membrane plasmique.
a) Jonctions serrées :
* terminologie : ces SJ sont encore appelés Zonula Occludens (Z0) car, dune part elles forment un anneau (ceinture) entourant le pourtour de la cellule (Zonula) et dautre part, elles permettant une occlusion complète de lespace intercellulaire (Occludens). Pour désigner les jonctions serrées on parle également de jonctions étanches, de jonctions imperméables ou de tight junctions. Les Jonctions serrées ne sont pas spécifiques des tissus épithéliaux mais on les observe essentiellement dans les tissus épithéliaux et dans les tissus apparentés aux tissus épithéliaux, (par exemple, les endothélium).
* ultrastructure : Au niveau des zonula occludens, les membranes cytoplasmiques des cellules adjacentes fusionnent sur de courtes distances au niveau de crêtes jonctionnelles encore appelées foyers de fusion. La juxtaposition de ces foyers de fusion conduit à la formation de lignes de fermetures. Ces lignes sentrecroisent et forment un réseau plus ou moins dense qui ceinture les cellules épithéliales et forme une zonula occludens. Cette ZO va constituer la « frontière » qui sépare, au plan physique et fonctionnel, le domaine apical du domaine baso-latéral (Cf infra).
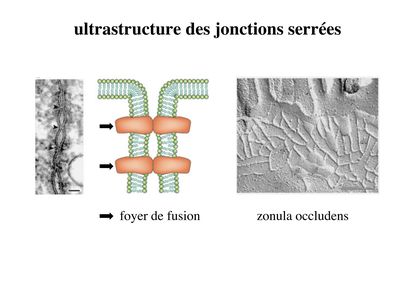
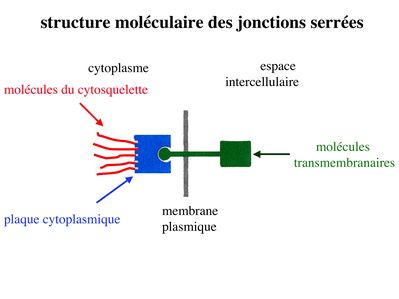
* structure moléculaire : trois catégories de molécules participent à la formation des jonctions serrées :
- des molécules transmembranaires qui au niveau des foyers de fusion vont interagir étroitement avec les molécules transmembranaires situées en vis-à-vis, à la façon dune fermeture éclair.
- des protéines dattachement intracellulaire sur lesquelles sarriment les molécules transmembranaires. Au sein des ZO, ces protéines dattachement forment ce que lon appelle la plaque cytoplasmique (ou plaque intracytoplasmique).
- des molécules du cytosquelette qui sinsèrent sur les protéines de la plaque.
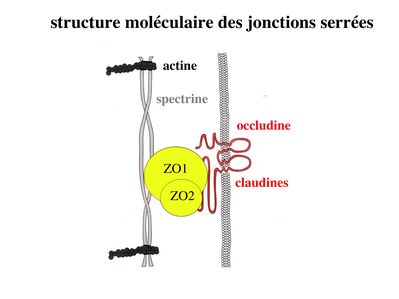
Il faut noter que cette organisation générale est également observée au niveau des jonctions dancrage, avec toutefois mise en jeu de molécules qui sont spécifiques aux jonctions dancrage. Dans les jonctions serrées, les principales molécules du domaine transmembranaire sont loccludine, les claudines et les JAM (plus récemment identifiées)(JAM = junctional adhesion molecules). Les molécules formant les plaques cytoplasmiques sont les protéines ZO-1 et ZO2. Les protéines du cytosquelette participant à la formation des jonctions serrées sont des microfilaments dactine (pour mémoire, ces filaments dactine sattachent aux plaques par lintermédiaire de molécules de spectrine ; la spectrine nest pas une molécule spécifique des globules rouges
).
* fonctions : dans les tissus épithéliaux, les ZO assurent 2 fonctions principales.
i) fonction dadhérence : les ZO maintiennent la cohésion des tissus épithéliaux en participant à ladhérence intercellulaire
ii) fonction de barrière : cette fonction sexerce au niveau de la membrane plasmique mais également au niveau de lespace para-cellulaire situé entre deux cellules épithéliales adjacentes. Au niveau de la membrane plasmique des cellules épithéliales, les jonctions serrées bloquent la circulation des protéines et des lipides au sein de la bi-couche lipidique. Les JS délimitent ainsi un domaine membranaire apical et un domaine membranaire basolatéral. Les JS bloquent également le flux de molécules et dions au niveau de lespace paracellulaire. Elles délimitent ainsi deux compartiments de compositions moléculaires distinctes : lun en regard du pôle apical et lautre en regard du pôle basal de la cellule. Le passage sélectif de certaines molécules à travers les JS reste toutefois possible, aussi bien dans lespace paracellulaire quau sein de la membrane plasmique.
b) Les jonctions dancrage : Elles ont la même structure générale que les jonctions serrées, mais permettent le passage des molécules dans lespace paracellulaire ou au sein de la membrane plasmique. On distingue 2 type de jonctions dancrage : les jonctions adhérentes et les desmosomes.
b-1 Les jonctions adhérentes :
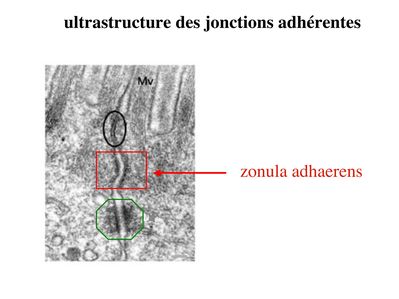
* ultrastructure : Dans les tissus épithéliaux, les jonctions adhérentes forment une ceinture dadhérence nommée Zonula Adhaerens qui est localisée juste en dessous de la Zonula Occludens. Dans les tissus non épithéliaux, les jonctions adhérentes sont très fréquentes mais prennent alors essentiellement la forme de points dunion nommés macula adhaerens. On trouve toutefois des Zonula Adhaerens dans un tissu non épithélial : le tissu musculaire myocardique.
* structure moléculaire : les principales molécules transmembranaires des jonctions adhérentes sont les molécules decadhérine. Il sagit dune famille de molécules comprenant la E-Cadhérine, initialment décrite dans les épithéliums, la N-Cadhérine initialement décrite dans les neurones, la P-Cadhérine initialment décrite dans le Placenta et la VE-Cadhérine initialement décrite dans les endothéliums. Ce sont des molécules dadhérences homophiliques (qui sassocient entre elles) et dont lactivité est calcium-dépendante (inactive en labsence de calcium). Parmi les cadhérines, on considère que la E-cadhérine joue un rôle essentiel dans le maintien de la morphologie et de la structure des tissus épithéliaux. Les plaques intra-cytoplasmiques sont formées de molécules de caténine (alpha, beta et gamma) et de plakoglobine. Limportance des forces de liaison associant les caténines aux Cadhérines dépend du degré de phosphorylation de caténines. Des signaux intracellulaires peuvent ainsi conduire au desassemblage des Zonula adhaerens par défaut dinteraction caténine-cadhérine. Dautres signaux intracellulaires, en particulier les GTPases, peuvent également perturber la fonction des Cadhérines, et en particulier la E-Cadhérine. Les éléments du cytosquelette sattachant aux plaques cytoplasmiques des jonctions adhérentes sont des microfilaments dactine, comme observés dans les jonctions serrées. (pour mémoire : toutefois, à la différence des jonctions serrées, ces microfilaments dactine sont orientés parallèlement à la membrane plasmique.)
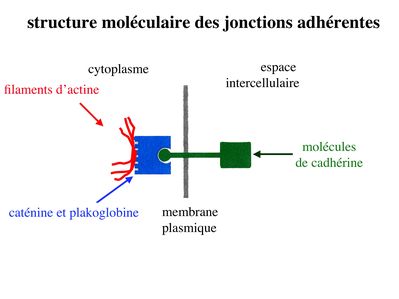
* fonctions : les Zonula Adhaerens permettent la constitution de réseaux intercellulaires de microfilaments dactine. On considère que le réarrangement coordonné de ces réseaux dactine joue un rôle important au cours du développement. Les Zonula Adhaerens ont également un rôle majeur dans le maintien de lhoméostasie du tissu épithélial (défaut de fonctions de la E-Cadhérine impliqué dans la cancérogénèse).
b-2 Les desmosomes :
* ultrastructure : il sagit de jonctions dancrage présentant une morphologie ultrastructural caractéristique en bouton pression. Dans les tissus épithéliaux, les desmosomes sont répartis de manière organisée dans la zone sous-jacente à la zonula adhaerens.
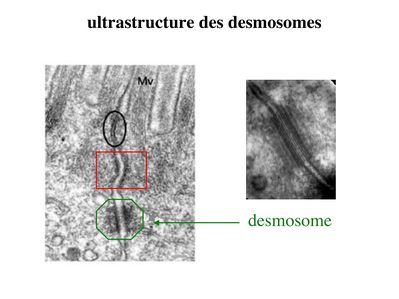
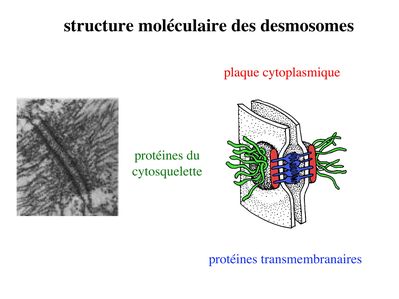
* structure moléculaire : Les molécules transmembranaires des desmosomes sont des cadhérines dun sous-type particulier et que lon nomme desmocolline et desmogléine. La plaque cytoplasmique est formée de molécules de plakoglobine et de desmoplakine. À la différence des jonctions serrées et des jonctions adhérentes, les éléments du cytosquelette reliés aux plaques cytoplasmiques des desmosomes sont des filaments intermédiaires. Dans les cellules épithéliales, il sagit toujours de filaments de cytokératine.
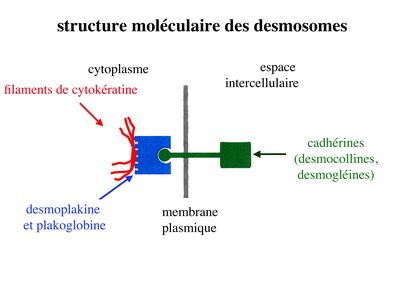
* fonctions : Dans les tissus épithéliaux, les desmosomes permettent la formation de réseaux intercellulaires de cytokératine. Ces réseaux participent à la cohésion architecturale du tissu épithélial et permettent la transmission et lamortissement des forces mécaniques sexerçant sur les cellules épithéliales.
c) les jonctions communicantes :
* ultrastructure : encore appelées gap junction, ces jonctions formées de petits canaux tubulaires permettant le passage de molécules entre cellules adjacentes. Ces jonctions sont présentes dans la plupart des tissus de l'organisme.
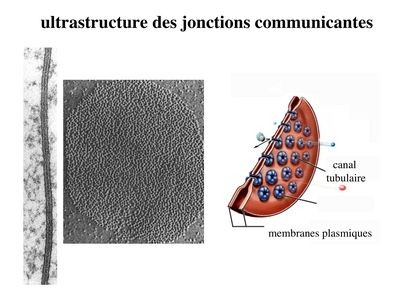
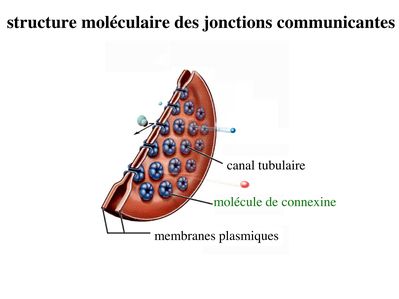
* structure moléculaire : contrairement aux autres systèmes de jonctions, les jonctions communicantes sont exclusivement formées de molécules transmembranaires qui ninteragissent pas avec des protéines cytoplasmiques ou des éléments du cytosquelette. Ces molécules transmembranaires appartiennent à la famille des connexines. Chaque cellule participant à la formation dun canal intercellulaire envoie un hémi-canal nommé connexon qui est constitué de 6 molécules de connexines assemblées en cylindre. Laboutement de deux connexons faisant saillie des membranes plasmiques de deux cellules adjacentes conduit à la formation dun canal tubulaire, formé de 12 molécules de connexines, qui traverse lespace intercelluaire. Les jonctions communicantes regroupent parfois plusieurs centaines de connexons qui se font vis-à-vis. Plusieurs dizaines de connexines ont été identifiés qui présentent chacune un patron dexpression tissu-spécifique.
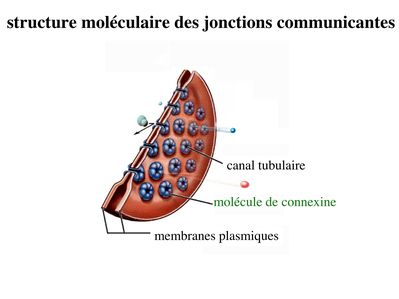
* fonctions : Les jonctions communicantes permettent le passage dions et de petites molécules de PM inférieur 1500 daltons. Le passage de seconds messagers intracellulaires tel que le calcium et lAMP cyclique permet une régulation coordonnée de lactivité cellulaire, on parle de couplage fonctionnel. La diversité moléculaire des connexines se traduit par une perméabilité sélective des jonctions gap. Selon leur type, les connexines sont perméables à des molécules de poids moléculaire et de charge électrique différents. Le Ph Cytosolique ainsi que la concentration intra-cytoplasmique de Calicium contrôlent le degré douverture des jonctions gap. Ces jonctions oscillent ainsi entre un état ouvert et un état fermé, comme les canaux ioniques conventionnels.
d) les complexes de jonction : la répartition des systèmes de jonctions dans les cellules épithéliales répond à une organisation stricte qui est spécifique des tissus épithéliaux. On appelle complexe de jonction le regroupement ordonné dans le domaine baso-latéral (mais à proximité du domaine apical) de la zonula occludens, de la zonula adhaerens et dune rangée parallèle de desmosomes. En dehors du complexe de jonction, on observe dans le domaine baso-latéral, une disposition apparemment aléatoire de jonctions gap et de desmosomes.

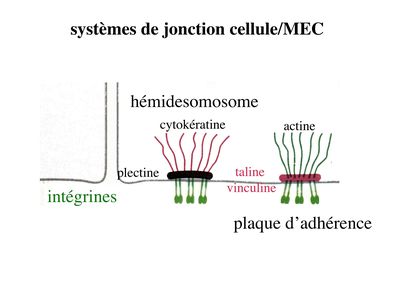
2) Systèmes de jonction cellule-MEC :
Ces SJ sétablissant entre cellules épithéliales et matrice de la lame basale. Ils sont de deux types : les hémi-desmosomes et les plaques dadhérences encores appelés contacts focaux. Leur structure générale est proche de celle des jonctions dancrage et des jonctions serrées : une molécule transmembranaire qui interagit avec une plaque cytoplasmique elle-même associée à des molécules du cytosquelette. Retenir que les molécules transmembranaires appartiennent à la famille des intégrines. Les intégrines sont une large famille de molécules reconnaissent des peptides portés par différentes molécules de la MEC (matrice extra-cellulaire). Parmi ces molécules, citons la fibronectine ou la laminine (Pour mémoire, la plaque cytoplamique est formée essentiellement de taline et de vinculine pour les contacts focaux et de plectine pour les hémidesmosomes. Par ailleurs, les contact focaux interagissent avec des microfilaments dactine et les hémidesmosomes avec des filaments intermédiaires de cytokératine).
3) Pathologies des systèmes de jonctions :
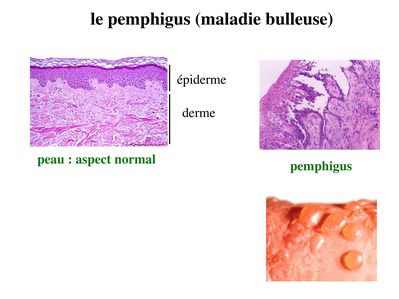
La principale pathologie des SJ actuellement identifiée est une maladie auto-immune de la peau nommée pemphigus ou maladie bulleuse. Chez les patients atteints de Pemphigus, on observe une dislocation de l'épiderme dont la conséquence est la formation de bulles. Des auto-anticorps antidesmogléines sont détectés dans le sérum de ces patients par technique dimmunohistofluorence. En bref, sur une coupe de peau normale set incubé du sérum de patients puis un Ac anti-Immunoglobuline humaine couplé à un fluorochrome.
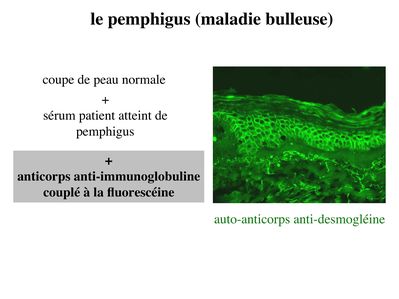
On considère actuellement quau moins deux autres types de pathologies épithéliales impliquent les systèmes de jonctions : les pathologies cancéreuses et les maladies infectieuses.
La cancérisation des tisus épithéliaux saccompagne fréquemment de mutations du gène de la E-Cadhérine ou dun défaut dexpression de la E-Cadhérine (passage de la forme E à la forme N). Les conséquence sont lacquisition dun caractère invasif de la cellule tumorale qui nest plus solidaire du reste de lépithélium. Par ailleurs, on observe une dissociation du couple Cadhérine/Caténine et la migration de la caténine vers le noyau elle est exerce une activité dinduction de la prolifération cellulaire.
Un certain nombre de pathogènes utilisent les molécules transmembranaires des systèmes de jonctions pour pénétrer dans les épithéliums et diffuser dans lorganisme.
C) Polarité
Si presque toutes les cellules de lorganisme présentent un certain degré d'asymétrie, les cellules épithéliales sont particulièrement polarisées et cette polarité sexprime aussi bien au plan morphologique, moléculaire que fonctionnel.
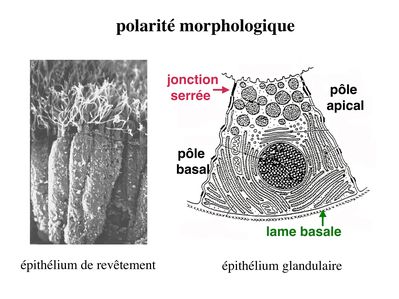
1) polarité morphologique : elle concerne la membrane plasmique et le cytoplasme. Au niveau de la membrane plasmique, plusieurs caractéristiques morphologiques différencient le domaine apical du domaine baso-latéral des cellules épithéliales. Ainsi, le domaine apical présente fréquemment des expansions cytoplasmiques de taille et de complexité variables allant des simples microvillosités aux cils vibratiles. Le domaine baso-latéral est le siège de nombreux systèmes de jonctions (intercellulaires ou entre cellule et matrice). Au niveau du cytoplasme, le pôle basal contient le noyau et lensemble des composants cellulaires nécessaires aux processus fondamentaux : mitochondries, REG, appareil de Golgi. Le pôle apical est parfois rempli de vésicules de sécrétion qui vont fusionner avec le domaine apical pour libérer leur contenu dans lespace extra-cellulaire (cellules épithéliales à activité sécrétoire).
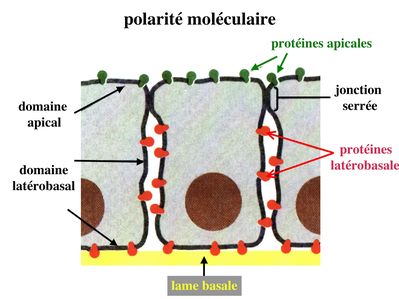
2) polarité moléculaire : Dans la membrane plasmique, la distribution et la circulation sont strictement maintenues au sein des deux domaines que sépare la zonula occludens : le domaine apical et le domaine baso-latéral. Les molécules membranaires sont synthétisées dans le cytoplasme puis triées a leur sortie du Glogi et adressées vers leur localisation membranaire apicale ou baso-latérale. Par ailleurs, cette distribution spécifique est maintenue par le blocage de circulation intra-membranaire, dun domaine vers lautre de la membrane plasmique, de manière bilatérale. Par contre, un passage trans-cytoplasmique, dun domaine membranaire vers lautre reste possible. Ce phénomène est nommé transcytose. Ces différents processus sont contrôlés de manière spécifique par chacun des éléments du cytosquelette. En particulier, les microtubules participent spécifiquement à ladressage des molécules du domaine apical et au phénomène de transcytose. Le phénomène de transcytose est mis à profit par le virus du SIDA (virus HIV) pour traverser la barrière épithéliale des muqueuses (génitales ou rectales) et infecter les cellules immunes localisées dans le tissu conjonctif sous-jacent à l'épithélium (chorion dans le cas des muqueuse, Cf cours N°2 sur le tissu épithélial).
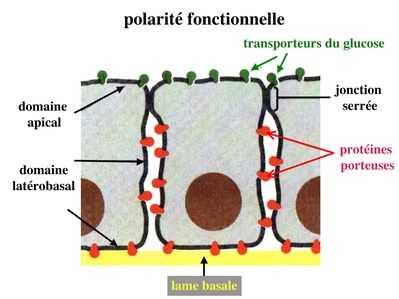
3) polarité fonctionnelle : elle découle des polarités morphologique et moléculaire. Un bon exemple de polarité fonctionnelle est fourni par les cellules épithéliales de lintestin grêle. La principale fonction de ces cellules est labsorption de nutriments i.e leur transport depuis la lumière intestinale vers le sang. Le pôle apical de ces cellules fait face à la lumière intestinale alors que le pôle basal est en contact avec la lame basale et la MEC sous-jacente au niveau de laquelle circulent des vaisseaux sanguins. La présence de JS impose que les nutriments empruntent la voie de passage transcellulaire depuis la lumière intestinale jusqu'à la MEC ou ils vont diffuser dans les vaisseaux sanguins. Si on prend lexemple du glucose, le passage transcellulaire du glucose nécessite ainsi deux types de protéines membranaires : i) des transporteurs actifs du glucose qui sont couplés au sodium et qui sont localisés dans le domaine apical des cellules ; ii) des protéines porteuses qui vont permettre la diffusion facilitée du glucose vers la MEC et l'espace paracellulaire basolatéral.
![]()