Le Tissu Conjonctif (cours N°1 et N°2, 2009)
Le Tissu Conjonctif
A) Généralités : Le tissu conjonctif non spécialisé (nommé tissu conjonctif) est présent dans la totalité des organes, avec toutefois des variations qualitatives et quantitatives majeures dun organe à lautre. Le cerveau par exemple est très pauvre en tissu conjonctif alors que le muscle est riche en TC. Le terme de tissu conjonctif désigne les tissus conjonctifs communs, non spécialisés. Il ninclut pas les tissus conjonctifs spécialisés cest-à-dire : le tissu adipeux, le tissu osseux et le tissu cartilagineux. On le verra plus loin, il existe néamoins différentes catégories de tissu conjonctif commune, non spécialisé. La matrice extra-cellulaire du TC est caractérisée par la présence de molécules fibreuses qui sont synthétisées par les cellules résidentes du tissu conjonctif : les fibroblastes. Selon sa localisation et son sous-type, le tissu conjonctif assure 3 fonctions principales : i) une fonction de soutien et de cohésion, liée à sa richesse en fibres ;
ii) une fonction nutritive et déchange, liée à sa richesse en matrice extracellulaire et en vaisseaux ;
iii) une fonction de défense, liée à la présence de cellules immune dites de passage.
Le terme de tissu conjonctif désigne les tissus conjonctifs communs, non spécialisés. Il ninclut pas le tissu adipeux, le tissu osseux et le tissu cartilagineux.
B) la matrice extra-cellulaire du tissu conjonctif
1) Notions générales sur les matrices extra-cellulaires : Tous les tissus sont formés par lassociation de cellules et dun milieu extra-cellulaire nommé matrice extra-cellulaire (MEC). Selon le tissu considéré, la MEC présente dimportantes variations quantitatives et qualitatives. Le tissu le plus riche en MEC est le tissu conjonctif et celui le plus pauvre en MEC est le tissu épithélial (La MEC y est en effet limitée à la matrice des espaces para-cellulaires et à la lame basale). Les MEC sont constituées principalement de 3 éléments : i) des fibres formées de lassemblage de protéines fibreuses dites de structure. Ces fibres ne sont présentes que dans la MEC des tissus conjonctifs et dans la MEC formant les lames basales. Elles sont visibles en microscopie électronique.
ii) de leau
iii) des molécules solubles tels que des sels minéraux, des polypeptides des sucres et des macromolécules protéiques. Leau et les molécules solubles forment la substance fondamentale. Celle-ci est dite optiquement vide i.e non visible en microscopie électronique.
2) Les molécules de la matrice : Les molécules participant à la MEC du tissu conjonctif peuvent être observées, pour partie ou en totalité, dans tous les types de matrice. Elles se divisent en 3 catégories : les polysaccharides, les protéines dadhérence et les protéines de structure. Seules les protéines de structure ont la capacité de former des fibres, les autres molécules (polysaccharides et molécules dadhérence appartiennent à la substance fondamentale.
a) polysaccharides ils sont répartis en deux familles.
* Les glycosaminoglycanes sont soit sulfatés (pour mémoire : chondroïtine-sulfate, le dermatane-sulfate, l'héparane-sulfate, le kératane-sulfate) soit non sulfatés (l'acide hyaluronique). Lacide hyaluronique présente la caractéristique de pouvoir lier de nombreuses protéines de la MEC du tissu conjonctif (pour mémoire : protéine fibreuses telle que le collagène, ou protéines d'adhérence telles que la fibronectine et la laminine). Lacide hyaluronique est également un ligand pour des récepteurs membranaires qui, dans le tissu conjonctif, sont exprimés par les fibroblastes et/ou par les cellules immunes de passage. Il sagit en particulier de la molécule CD44 et des molécules de la famille Toll-like Receptor (TLR). On considère que linteraction entre acide hyaluronique et ses récepteurs membranaires joue un rôle essentiel dans les processus dinflammation et de réparation tissulaire, au sein du tissu conjonctif (Rappel : dans les tissus épithéliaux, l'acide hyaluronique présent dans la lame basale interagit avec la molécule CD44 exprimée par les cellules épithéliales).
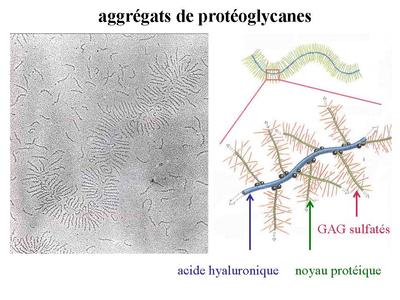
* Les protéoglycanes sont formés par un noyau protéique sur lequel se lient des glycosaminoglycanes sulfatés. Ces protéoglycanes (pour mémoire : syndecan, perlecan) forment des aggrégats de très grande taille dont le squelette est formé de molécules d'acide hyaluronique et qui ont la capacité de fixer certaines cytokines ou facteurs de croissance et donc de moduler leur biodisponibilité (pour mémoire: les aggrégats de protéoglycanes s'articulent autour de molécules d'acide hyaluronique).
 b) les protéines d'adhérence : comme les polysaccharides, ce sont des molécules solubles entrant dans la composition de la substance fondamentale.
* la fibronectine :
* la laminine : il s'agit d'une protéine d'adhérence présente dans les tissus conjonctif bien quessentiellement localisée au niveau des lames basales
mais qui est prédominante au niveau des lames basales et non du TC. Elle lie certains polysaccharides tel que l'acide hyaluronique ainsi que les récepteurs membranaires de la famille des intégrines.
c) les protéines de structure :
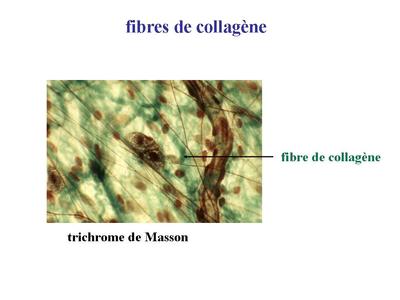
* le collagène : cest la plus abondante des protéines de lorganisme et on considère quelle constitue un quart du poids sec des mammifères. On reconnaît actuellement plus de 20 types de molécules de collagène. Le collagène I est le plus abondamment distribué dans le tissu conjonctif. Les molécules de collagène I forment des microfibrilles visibles en microscopie électronique et présentant une striation transversale due à l'alternance de bandes sombres et claires.
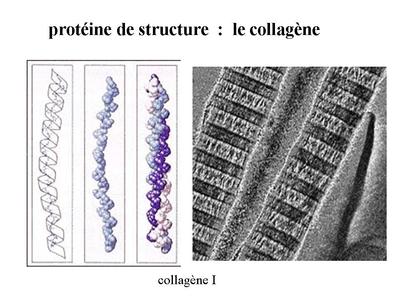 Ces microfibrilles se groupent pour former des fibres qui s'assemblent en faisceaux diversement orientés dans lespace . Cette organisation confère des propriétés de soutien mécanique au tissu conjonctif. Ces fibres et faisceaux sont visibles en MO après coloration au jaune safran ou au trichrome de Masson.
Une catégorie de tissu conjonctif, le tissu conjonctif réticulaire, contient majoritairement du collagène de type III et non de type I ; Le collagène type III forme des fibres dites de réticuline qui ne sont pas visualisables par le trichrome de Masson ou le jaune safran.
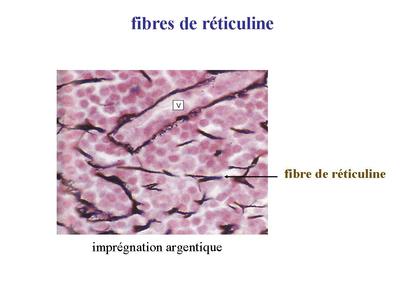 Par ailleurs, il faut retenir que le collagène de type II est caractéristique du tissu cartilagineux et que le collagène de type IV est essentiellement présent au niveau des membranes basales.
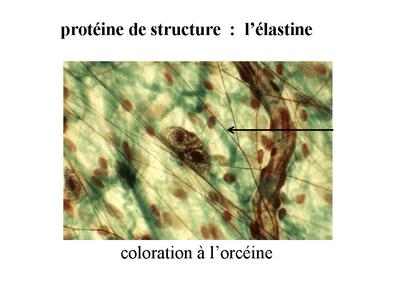
* lélastine : cest la molécule principale des fibres élastiques qui sont présentes dans les tissus conjonctifs élastiques. En MO, les fibres élastiques sont visibles par la coloration à lorcéine sous forme d'un réseau de fines fibres allongées et anastomosées.
 C) Cellules du tissu conjonctif :
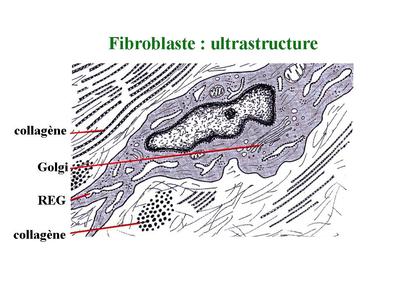
1) fibroblastes : le fibroblaste est le seul type cellulaire présent dans tous les tissus conjonctifs (TC communs, non spécialisés). Il s'agit d'une cellule fusiforme, porteuse de prolongements plus ou moins ramifiés. En microscopie électronique, le cytoplasme des fibroblastes est riche en organites impliqués dans la synthèse protéique : il s'agit d'une cllule sécrétrice de protéines. Les fibroblastes synthétisent la matrice du tissu conjonctif et sont le plus souvent entourés des protéines fibreuses dont ils sécrètent les molécules précurseurs. Cest le cas notamment du pro-collagène et de la pro-élastine qui sont les formes non fibrillaires du collagène et de lélastine.
Le terme de fibrocyte désigne des fibroblastes en fin de vie qui ne sont plus capables de division cellulaire et synthétisent peu de matrice. Les fibroblastes dérivent de cellules souches mésenchymateuses. Ces cellules sont à lorigine de tous les types cellulaires spécifiques des tissu conjonctifs spécialisés ou non spécialisés : les fibroblastes (qui se différencient en fibrocytes), les adipoblastes (qui donnent les adipocytes), les chondroblastes (qui génèrent chondrocytes) et les ostéoblastes (a lorigine des ostéocytes). Chez l'adulte, des travaux récents montrent que les cellules souches mésenchymateuses i) persistent dans les tissus conjonctifs non spécialisés (dans le tissu conjonctif associé à la moelle osseuse par exemple) ii) présentent un potentiel de différentiation plus large quinitialement observés (potentiel de différentiation neuronale par exemple). Par ailleurs, certains auteurs ont récemment mis en évidence l'existence de précurseurs sanguins des fibroblastes, précurseurs qui seraient recrutés sur les sites inflammatoires et participeraient à la reconstruction tissulaire ou à la formation de lésions cicatricielles fibrotiques (fibros cicatricielle).
La synthèse protéique des fibroblastes ne se limite pas à la sécrétion de molécules de la matrice. Outre les molécules de la MEC. Les fibroblastes synthétisent des cytokines et notamment de linterféron-beta qui joue un rôle important dans les défenses anti-virales. Ils synthétisent également des cytokines pro-inflammatoires et des chimiokines qui participent au micro-environnement des tumeurs. Le rôle permissif de ce micro-environnement inflammatoire est fortement suspecté (facilitation de linvasion et de la dissémination métastatique).
2) adipocytes : ce sont des cellules spécialisées dans la mise en réserve des lipides. Les adipocytes sont regroupées en amas au sein de la plupart des tissus conjonctifs non spécialisés. Le terme de tissu adipeux désigne un tissu conjonctif spécifique au sein duquel les adipocytes sont très largement majoritaires. Les adipocytes sont de morphologie sphérique ou polyédrique avec un cytoplasme essentiellement occupé par une vacuole lipidique et un petit noyau refoulé contre la membrane plasmique. Les adipocytes ne sont pas de simples cellules de stockage lipidique.
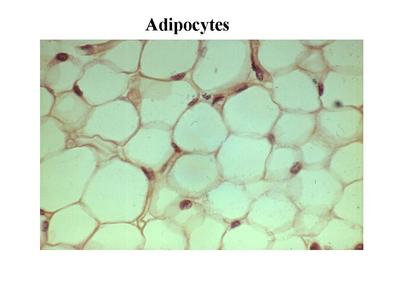 Les adipocytes synthétisent un grand nombre de molécules contrôlant le métabolisme lipidique, la prise alimentaire et la réponse immune. Certains auteurs parlent dadipokines pour désigner ces molécules. Ainsi, la leptine, synthétisée par les adipocytes, est relarguée dans le sang et agit au niveau de récepteurs hypothalamiques pour réguler la sensation de satiété. De la même façon, les adipocytes sont une importante source de TNF-alpha (tumor necrosis factor-alpha), cytokine pro-inflammatoire impliquée dans lamaigrissement prononcé observé au cours des stades terminaux du cancer. Laugmentation massive du volume du tissu adipeux est une caractéristique de lobésité sévère (encore appelée obésité morbide). On a longtemps considéré que les adipocytes pouvaient être soumis à des variations de volume mais non de nombre. En fait, au cours des obésités sévères (obésités dites « morbides »), il existe une augmentation du nombre dadipocyte qui serait lié à une différenciation adipocytaire de cellules souches mésenchymateuses résidant dans le tissu adipeux. Par ailleurs, lobésité sévère saccompagne dune infiltration du tissu adipeux par des macrophages et par une altération du statut immunitaire des patients.
3) cellules immunes : Les tissus conjonctifs dits lâches, c'est-à-dire riches en cellules et pauvres en fibres (Cf infra), sont dimportants lieux de transit pour les cellules immunes sanguines. Selon la localisation du tissu conjonctif lâche, on observe des variations qualitatives et quantitatives de ces populations cellulaires immunes. Ces variations sont corrélées à des statuts immunitaires différents. Par exemple, le chorion de la muqueuse intestinale (c'est-à-dire le tissu conjonctif sous-jacent à lépithélium intestinal) contient de nombreux lymphocytes T et des plasmocytes sécrétant des Immunoglobulines de type A. Par comparaison, le derme (le tissu conjonctif sous-jacent à lépiderme) contient des cellules dendritiques (les cellules dendritiques du derme sont à distinguer des cellules de Langerhans de lépiderme), des lymphocytes T mais pas de plasmocytes .
a) les macrophages : ils dérivent de monocytes sanguins ayant pénétrés dans les tissus conjonctifs lâches. Ils présentent 4 caractéristiques morphologiques principales :
i) il sagit de cellules rondes ou ovalaires de très grande taille (diamètre de 50 micron ou plus alors que les monocytes ont un diamètre inférieur à 20 microns)
ii) leur noyau est excentré et présente une morphologie réniforme ou encochée
iii) lappareil vacuolaire y est très développé et comprend des vésicules de pinocytose, des lysosomes primaires, des phagosomes et des phagolysosomes
iv) on observe des expansions de la membrane plasmique formant des pseudopodes. Ces pseudopodes sont nécessaires à la mobilité des macrophages.
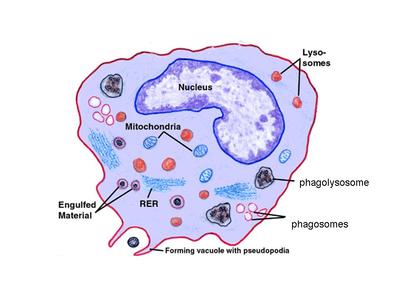 Les macrophages exercent principalement 3 fonctions. La première est la phagocytose. Elle sexerce vis-à-vis de micro-organismes, de débris cellulaires, de cellules en apoptose et dantigènes associés à des anticorps (complexes antigène/anticorps). Cette activité met en jeu un ensemble de récepteurs membranaires capables de reconnaître spécifiquement les cibles à phagocyter. Par ailleurs, selon le recepteur membranaire impliqué, la fonction de phagocytose est couplée à une activation cellulaire dont les caractéristiques sont spécifiques du récepteur. La deuxième fonction des macrophages est la présentation dantigènes aux lymphocytes T. Elle nécessite une phase dite dapprêtement de lantigène. Il s agit dune digestion sélective de lantigène conduisant à la formation de multiples peptides qui seront présentés à la surface membranaire en association avec les molécules dhistocompatibilité. Cette phase dapprêtement est accompagnée dune phase de migration des macrophages depuis le TC jusquaux ganglions lymphatiques ou seffectue linteraction avec le lymphocyte T. La troisième fonction est la synthèse de cytokines pro-inflammatoires permettant lamplification de la réponse immune. Cest le cas notamment de lIL-1 (interleukine-1), de l'IL-6 (interleukine-6) et du TNF-alpha. Il faut noter toutefois que certains signaux dactivation des macrophages conduisent au contraire à la synthèse de cytokines dites anti-inflammatoires (pour mémoire : linterleukine 10). b) les plasmocytes : les plasmocytes correspondent au stade ultime de différenciation des lymphocytes B et sont les seules cellules du système immunitaire capables de sécréter des immunoglobulines. Il sagit de cellules ovoïdes dont le noyau excentré présente une chromatine dite « en rayons de roue ». Les plasmocytes possèdent un volumineux appareil de Golgi et un réticulum endoplasmique granuleux abondant.
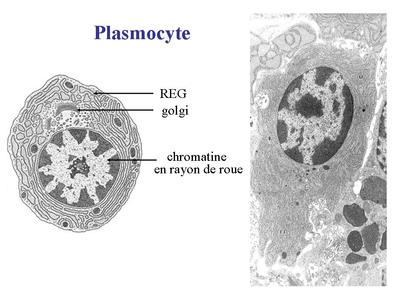 Les plasmocytes sont des cellules non circulantes (cest-à-dire non présentes dans le sang), présentes exclusivement au niveau des tissu conjonctifs lâches, des organes lymphoïdes secondaires (ganglions, rate) et de la moelle osseuse (organe lymphoïde primaire). c) les mastocytes : ce sont des cellules arrondies, à noyau central, et caractérisées par la présence dabondants grains de sécrétions intracytoplasmiques. Ces grains (encore nommés granulations) contiennent essentiellement de lhistamine qui est une molécule fortement vaso-active.
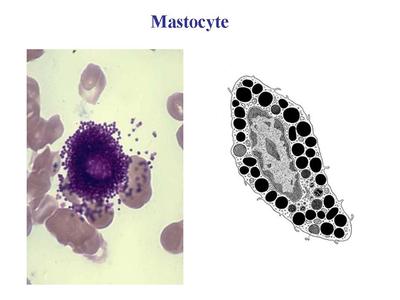 La dégranulation des mastocytes cest-à-dire la libération du contenu des granulations, par exocytose, est induite principalement par la fixation dimmunoglobulines de type E (Ig E) à des récepteurs membranaires spécifiques (recepteuirs aux IgE). Elle intervient lors de phénomènes allergiques aigus en induisant une vasodilation locale avec infiltration massive de cellules immunes sanguines au sein du tissu conjonctif. 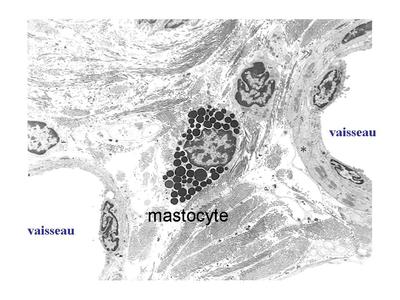 Les mastocytes sont particulièrement abondants dans le tissu conjonctif de la peau (derme, hypoderme), des bronches et des voies digestives. Cette localisation préférentielle explique leur rôle dans la physiopathologie de maladies allergiques cutanées (eczema, urticaire), pulmonaires (asthme) ou digestives (allergies alimentaires). Dans ces pathologies, les traitements antihistaminiques sont largement utilisés. D) Classification
Il existe 4 catégories de TC non spécialisé : le TC lâche, le tissu conjonctif réticulaire, le TC dense et le TC élastique.La classification des tissus conjonctifs non spécialisés est basée sur 2 critères : i) la richesse relative en fibres par rapport à la richesse en cellules et en substance fondamentale ; ii) la nature des fibres.
1) le tissu conjonctif lâche :
a) généralités : Cest le tissu conjonctif le plus répandu dans lorganisme.
Il est relativement pauvre en fibres comparés aux tissus conjonctifs denses. En revanche il est riche en cellules et/ou en substance fondamentale. Par ailleurs il est richement vascularisé. Il exerce principalement des fonctions de défense immune, de soutien nutritif et métabolique et de soutien mécanique. On retient 4 principales catégories de TC lâche :
i) les TC sous-jacents aux épithéliums de revêtement i.e ; le derme et lhypoderme au niveau de la peau et le chorion au niveau des muqueuses ;
ii) le TC de la paroi des veines et des artères de faible calibre;
iii) le tissu conjonctif associé aux nerfs périphériques et aux muscles ;
iv) le TC du parenchyme des organes pleins et qui est nommé stroma conjonctif.
Tous les organes pleins comme le rein le foie ou le pancréas contiennent un abondant tissu conjonctif qui rempli les interstices entre cellules et assure la cohésion de lorgane. On peut dire que le parenchyme des organes pleins est constitué de cellules spécialisées et dun stroma conjonctif. Une exception à cette règle : le parenchyme du système nerveux central. A retenir toutefois quon trouve du TC dans le système nerveux central, au niveau de la paroi des vaisseaux sanguins non capillaires. b) Un exemple de tissu conjonctif lâche : le derme et lhypoderme.
* Le derme est dépaisseur variable selon la région cutanée, pouvant aller de 0,3 mms à 3 mms. Il est subdivisé en 2 zones.
i) la zone superficielle du derme sinsinue entre les replis des couches profondes de lépiderme. On la nome derme papillaire.
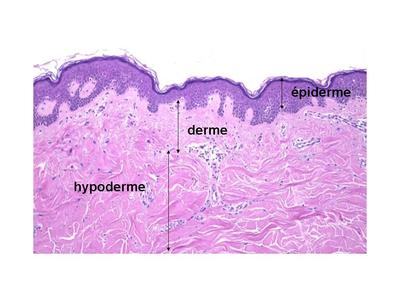 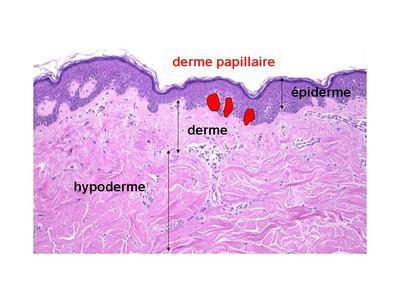 Le derme papillaire est formé principalement de fibroblastes qui sont entourés de fibres de collagène type I, de fibres délastine et de SF. Les fibres de collagène ne forment pas de faisceaux, et les fibres délastine sont très fines. Les fibres délastine sont disposées perpendiculairement à la jonction dermo-épidermique et disparaissent au cours du vieillissement cutané (raréfaction après 30 ans, disparition après 40 ans). ii) le derme profond est nommé derme réticulaire. A la différence du derme papillaire, les fibres de collagène sy organisent en faisceaux, les fibres délastine adoptent une disposition parallèle à la jonction dermo-épidermique et ont un diamètre plus important.
Quelque soit son sous-type (papillaire ou profond), le derme présente 3 caractéristiques essentielles : il accueille de nombreuses cellules immunes de passage, son innervation et sa vascularisation sont riches, il contient des glandes sudoripares et des follicules sébacés.
- Les cellules immunes du derme : il sagit principalement de cellules dendritiques (à ne pas confondre avec les cellules de Langerhans de lépiderme), de macrophages, de mastocytes et de lymphocytes T ou B. Le derme contient en revanche très peu de plasmocytes, ce qui constitue une différence essentielle avec le chorion des muqueuses (digestives, respiratoires, uro-génitales) qui contient de nombreux plasmocytes (rappel : les plasmocytes des muqueuses synthétisent préférentiellement des immunoglobulines de type A).
- La vascularisation du derme : le derme renferme un réseau capillaire anastomosé au réseau artério-veineux de lhypoderme (rappel : lépiderme est avasculaire). Les capillaires du derme sont de type continu (jonctions serrées de type macula occludens, lame basale continue). Le derme renferme également des vaisseaux lymphatiques qui sanastomosent entre eux au niveau du derme papillaire. Cest par cette circulation que les cellules présentatrices dantigènes de la peau (Langerhans, cellules dendritiques du derme, macrophages du derme) ainsi que les lymphocytes circulant dans le derme rejoignent les ganglions lymphatiques de la zone cutanée drainée.
L'innervation du derme : le derme renferme des nerfs végétatifs et des nerfs sensitifs. Les nerfs végétatifs sont destinés aux vaisseaux, aux muscles arecteurs des poils et aux glandes sudoripares. On observe également des fibres nerveuses sensitives qui sont de deux grands types :
i) des fibres permettent la perception des variations de température et la nociception (perception de la douleur). Ces fibres sont toujours amyéliniques et présentent des terminaisons libres qui sont disséminées dans le derme superficiel et dans les couches profondes de lépiderme (lépiderme est avsaculaire mais il est innervé, Cf brulûres premier degré).
ii) des fibres nerveuse permettant la perception du toucher. Ces fibres sont myélinisées ou non myélinisées. Leurs terminaisons axonales sont organisées au sein corpuscules sensoriels localisés dans le derme (absent de lépiderme). Ces fibres sont sensibles aux forces mécaniques induits par le contact léger, la pression, les vibrations, les mouvements. Par ailleurs, un contingent de ces fibres mécanoréceptrices fait synapse avec les cellules de Merckel dans la couche basale de lépiderme (doù la sensibilité tactile particulière des mains et des pieds).
Dernière caractéristique du derme, il renferme lappareil pilo-sébacé et les glandes sudoripares. Lappareil pilo-sébacé est constitué par lassociation de trois éléments :
i) un follicule pileux qui contient la base du poil et qui est localisé dans le derme papillaire
ii) une glande sébacée qui sécrète le sébum (Rappel : le sébum est formé de lipides et de débris cellulaires ; sa sécrétion se fait sur le mode holocrine. Pour mémoire : le contrôle de la sécrétion sébacée est essentiellement hormonal ; lacnée correspond à une obturation, partiellement hormono-dépendante, du canal excréteur des glandes sébacées)
iii) un muscle arecteur du poil (innervation végétative).
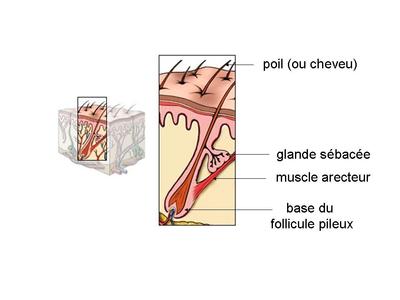 Par ailleurs, lappareil pilo-sébacé contient des cellules souches capables de régénérer les glandes sébacées, les follicules pileux mais également lépiderme. Ces cellules souches présentent donc un potentiel de différentiation plus large que les cellules souches de la couche basale de lépiderme. Les cellules souches de lappareil pilo-sébacé sont localisées dans zone bien spécifique, le bulge, qui forme une niche située à proximité des glandes sébacées. 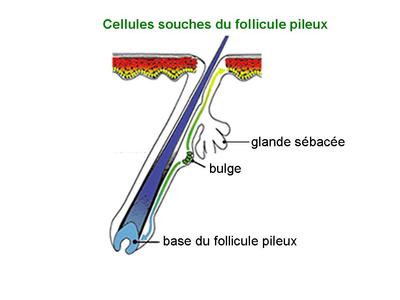 Les glandes sudoripares sont annexées au follicule pileux et sont responsables de la sécrétion de la sueur.
* lhypoderme : il est richement vascularisé et innervé mais ne contient pas ou peu de cellules immunes de passages, pas de corpuscules sensoriels, pas dappareil pilo-sébacé ni de glandes sudoripares. Lhypoderme est en revanche riche en adipocytes formant ce quon appelle le pannicule adipeux.
2) le tissu conjonctif réticulaire ou réticulé :
a) généralités :
Il est pauvre en fibres et ses fibres sont exclusivement des fibres de réticuline. Il est présent dans le parenchyme des organes hématopoïétiques suivants : rate et ganglions lymphatiques. Le TC réticulaire est également présent dans la moelle osseuse mais il est absent du thymus. Enfin, on le trouve dans le parenchyme hépatique. Il faut noter que dans le foie, la rate et les ganglions lymphatiques du tissu conjonctif dense forme une capsule externe et des parois internes délimitants des lobules.
b) un exemple : le tissu conjonctif réticulé des ganglions lymphatiques Les ganglions lymphatiques sont de petits organes en forme de haricot au niveau desquels les vaisseaux lymphatiques sanastomosent. Leur taille varie de quelques millimètres à plusieurs centimètres en fonction de leur état de stimulation (activation = augmentation de taille). Ils constituent un site de confluence et dinteraction pour les cellules et les molécules qui circulent dans les vaisseaux lymphatiques. On parle de système de drainage lymphatique pour désigner la circulation des cellules et des molécules immunes depuis les organes non hématopoïétiques vers les ganglions. Ce système de drainage lymphatique est présent dans lensemble de lorganisme à lexception du système nerveux central (cest lune des particularités du statut immunitaire spécifique au système nerveux central). A noter que les ganglions sont reliés entre eux par les vaisseaux lymphatiques et que la lymphe se jette dans la circualations sanguine par labouchement du canal thoracique (gros vaisseaux lymphatique traversant labdomen) à la veine sous-clavière gauche. Les fibres de réticuline forment la charpente des ganglions lymphatiques. Elles exercent un rôle de soutien mécanique (charpente) et orientent la circulation du flux lymphatique de la périphérie vers le centre du ganglion cest-à-dire depuis les vaisseaux lymphatiques afférents vers le canal lymphatique efferent. Par ailleurs les fibres de réticuline permettent larrimage dun riche réseau de macrophages et de cellules dendritiques résidentes dont la fonction est le filtrage de la lymphe (phagocytose des débris, particules et micro-organismes) et la presentation dantigènes aux lymphocytes T et B. 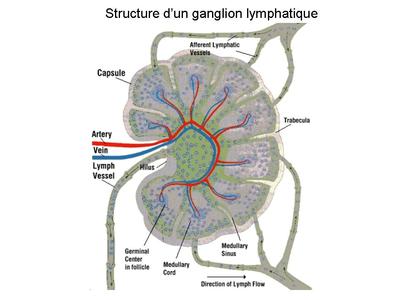 3) le tissu conjonctif dense (ou fibreux) :
a) généralités : Il est riche en fibres et pauvre en cellules et substance fondamentale. Les fibres de collagène occupent lessentiel du volume des tissu conjonctifs denses et leur confèrent des propriétés de résistance mécanique.
Lorsque les fibres de collagène sont orientées en faisceaux parallèles, on parle de tissu conjonctif dense orienté. Ce tissu conjonctif est observé au niveau des tendons, des ligaments et de la cornée. La vascularisation y est très pauvre ce qui limite les capacités de cicatrisation de ces tissus.
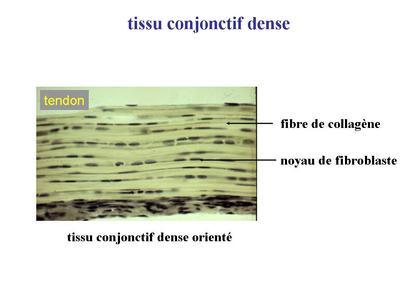 Lorsque les fibres de collagène ne sont pas orientées de manière ordonnée, on parle de tissu conjonctif dense non orienté. Ce tissu conjonctif est observé au niveau des parois conjonctives délimitant les organes pleins (dont le foie), dans les capsules articulaires et au pourtour de los (périoste). b) un exemple : le tissu conjonctif de la cornée. Schématiquement, la cornée est formée dun épithélium cornéen (pavimenteux stratifié non kératinisé) qui repose sur un tissu conjonctif dense orienté, nommé stroma de la cornée (pour mémoire : la face postérieure de la cornée est formée d'un épithélium siple nommé "endothélium"). 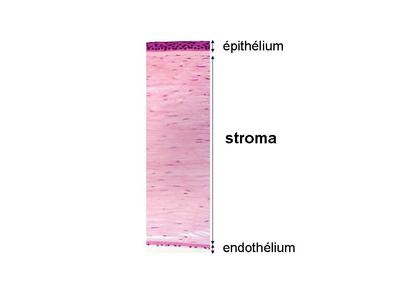 Ce tissu conjonctif constitue 90% de lépaisseur de la cornée. Il est formé de faisceaux de fibres de collagènes type I qui sorganisent en lamelles (il y a une cinquantaine de lamelles dans la cornée). Au sein de chaque lamelle, les fibres de collagène sont orientées parallèlement les unes par rapport aux autres. Dune lamelle à lautre, les fibres ont une orientation différente, empêchant ainsi tout phénomène de polarisation de la lumière transmise à travers la cornée. Entre les lamelles se trouvent des fibrocytes, très aplatis et au cytoplasme réduit. 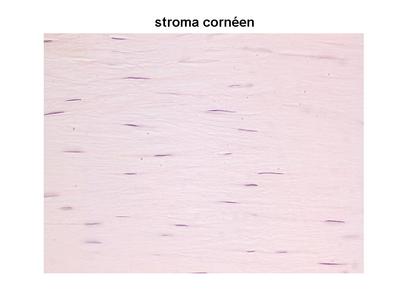 4) le tissu élastique :
a) généralités : Certains auteurs le considèrent comme une variété de TC dense comprenant des fibres de collagène et des fibres délastine. Ces fibres élastiques sorganisent et se regroupent fréquemment sous forme de lames élastiques. On observe essentiellement ce type de TC au niveau de la paroi des artères de gros calibre tel que laorte (rappel : la paroi des artères de faibles calibres et des veines est essentiellement formée de tissu conjonctif lâche).
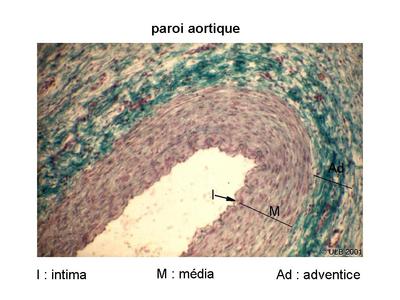
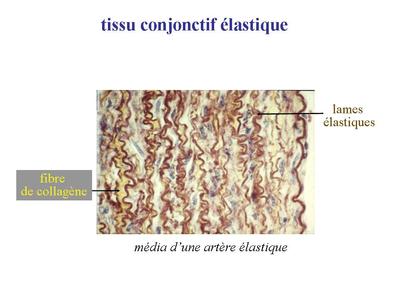 b) un exemple de TC élastique : la paroi de laorte
Laorte est une artère dite de type élastique par opposition aux artères de type musculaire qui correspondent aux artères de moyen calibre. La paroi de laorte est composée de 3 couches. De lintérieur vers lextérieur on distingue lintima formé par les cellules endothéliales reposant sur une lame basale, la média formée de tissu conjonctif élastique et de cellules musculaires lisses, ladventice qui est une couche de tissu conjonctif lâche qui contient des vaisseaux, des nerfs et des cellules immunes de passage (macrophages essentiellement). Le tissu conjonctif de la média contient peu de fibroblastes mais beaucoup de fibres. Il sagit essentiellement de fibres délastine qui sorganisent en lamelles épaisses, et concentriques séparées par des interstices (fenestration des lames délastine). Dans les interstices, se trouvent des cellules musculaires lisses, de rares fibroblastes et de la substance fondamentale. On considère que les lames élastiques occupent le tiers du volume de la média aortique. Par comparaison aux artères élastiques, la média des artères musculaires, est essentielement formée de cellules musculaires lisses et contient des fibres délastine qui ne sont pas ou peu organisées en lames.
 E) Pathologies du tissu conjonctif :
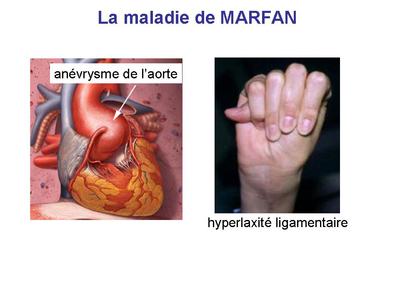
1) la maladie (ou syndrome) de Marfan
La maladie de Marfan est une maladie génétique autosomique dominante, cest à dire quelle touche aussi bien les hommes que les femmes, et que lenfant dun sujet atteint présente un risque de 50% dêtre atteint à son tour. Elle est due le plus souvent à latteinte du gène de la fibrilline. La fibrillne est une protéine fibreuse de la matrice extra-cellulaire des tissus conjonctif. Elles est présente dans tous les TC mais est particulièrement abondate dans le TC élastique. La maladie de Marfan est une pathologie très polymorphe au cours de laquelle on peut observer à des degrés variables :
i) une morphotype longiligne et une hyperlaxité ligamentaire,
ii) une atteinte occulaire secondaire à une sub-luxation du cristallin (le cristallin est maintenu par des structures pseudo-ligamentaires formées de TC fibreux)
iii) une atteinte cardiovasculaire (chez 60% des patients) et principalement un anévrysme aortique nécessitant une intervention chirurgicale.
 2) lanévrysme aortique :
La principale cause danévrysme aortique est lathérosclérose. A un stade évolué dathérosclérose on observe 3 phénomènes qui peuvent être responsables dune dilatation localisée de la paroi aortique : i) une infiltration de la média par des dépôts de lipides et par des macrophages remplis de lipides (macrophages spumeux), ii) une réaction fibrotique au contact de ces dépôts (prolifération fibroblastique et synthèse de collagène), iii) une dégénérescence des fibres élastiques et des cellules musculaires. Les anévrysmes de l'aorte abdominale sont les plus fréquents mais ceux de l'aorte thoracique peuvent être très volumineux et présente un risque de rupture important.
Modifier - Historique des modifications - DerniersChangements |
Site créé avec ViaBloga
-- Modèle rdc par Jon Roobottom,
Paul Lloyd et
Stéphane Gigandet --
![]()