
LES EPITHÉLIUMS DE REVETEMENT
A) définitions : il existe deux grandes catégories de tissus épithéliaux : les épithéliums de revêtement et les épithéliums glandulaires. Les épithéliums de revêtement sont des tissus de surface exerçant des fonctions de barrière, de protection et, parfois, dabsorption. Les épithéliums glandulaires sont le plus souvent enchassés dans les organes ou forment des organes glandulaires
B) terminologie : les épithéliums de revêtement au sens strict du terme regroupent lépiderme et les épthéliums muqueux. Ils ont pour caractéristique commune de reposer sur une couche de tissu conjonctif dont l'épaisseur est au moins égale à celle de l'épithélium. Par ailleurs, un certain nombre de tissus sont considérés comme apparentés aux tissus épithéliaux de revêtement car ils n'en présentent pas toutes les caractéristiques: il sagit des endothéliums, des mésothéliums et des épithéliums sensoriels.
1) lépiderme : il sagit de lépithélium recouvrant la surface externe de lorganisme. Il a une structure uniforme et constitue la couche superficielle de la peau. Lépiderme repose sur 2 couches de tissu conjonctif qui sont, de la superficie vers la profondeur : le derme et lhypoderme.
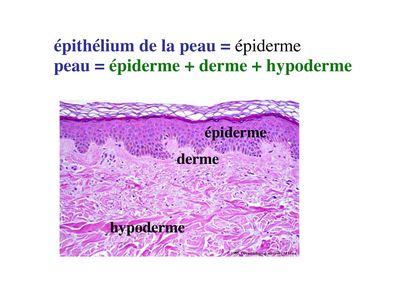
2) les épithéliums muqueux : les muqueuses recouvrent la surface interne des organes creux qui sont en continuité avec le milieu extérieur : voies urogénitales, voies aériennes supérieures et inférieures, tube digestif. Le terme de muqueuse désigne lassociation dune couche de tissu épithélial de revêtement et dune couche de tissu conjonctif sous-jacent, nommé chorion (attention : la lame basale est partie intégrante du tissu épithélial et nappartient pas au tissu conjonctif ; cest une organisation particulière de la matrice extra-cellulaire du tissu épithélial). Les épithéliums muqueux (et les muqueuses) sont nommés par leur localisation (par exemple : épithélium oesophagien, épithélium bronchique, urothélium). Chacun deux à une structure propre qui est caractérisée principalement par le nombre, la morphologie et les fonctions des cellules épithéliales qui la composent. 
3) tissus apparentés aux épithéliums de revêtement : ces tissus sont dits apparentés aux tissus épithéliaux car ils ne présentent pas lensemble des caractéristiques communes aux tissus épithéliaux. En particulier : ils reposent sur une couche fine de tissu conjonctif, leur lame basale est parfois discontinue, l'expression de cytokératine est inconstante, les complexes de jonctions sont absents.
a) les mésothéliums : ils participent à la formation des tuniques séreuses de lorganisme cest-à-dire le péritoine, les plèvres et le péricarde. Les éreuse recouvrent des organes (coeur poumons) ou groupes d'organes (organes abdominaux) qui, dans leur fonctionnement normal, ont la caractéristique de s'expandre (respiration, battements cardiaques, peristaltisme intestinal). Les séreuses sont toutes organisées sur le même mode : i) un feuillet viscéral, en contact direct avec le s organes abdominaux, les poumons ou le myocarde, ii) un feuillet pariétal, qui entoure le feuillet viscéral. Chaque feuillet est formé dun mésothélium reposant sur une fine couche de tissu conjonctif nommée couche sous-mésothéliale.
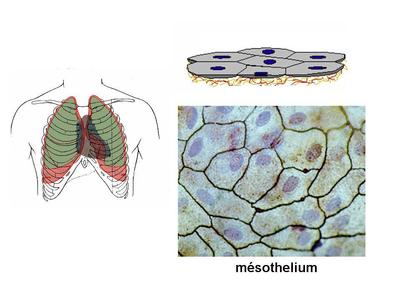
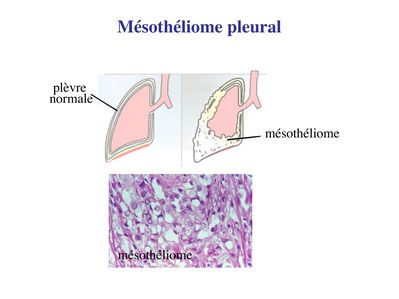
Dans chaque séreuse, les mésothéliums se font visà-vis et les glissements de la couche viscérale sur la couche pariétale permettent aux séreuses de sadapter aux variations de volume des organes quelles entourent. Ces mouvements sont facilités par la présence dune très fine couche liquidienne. En situation pathologique, on peut observer une augmentation du volume de ce liquide conduisant à la formation dun épanchement (pleural, péritonéal, péricardique). Un exemple est donné par la péricardite virale (infection virale du péricarde) qui se traduit par la formation dun épanchement péricardique à lorigine de douleurs thoraciques et dun frottement à lauscultation. Une augmentation importante de cet épanchement peut conduire à une limitation des battements cardiaques; on parle de tamponade cardiaque. Les mésothéliums peuvent être le siège de tumeurs malignes, les mésothéliomes (ou mésothélioma), dont le plus fréquent est le mésothéliome de la plèvre. Il sagit dun cancer dune très haute malignité (survie moyenne inférieure à 1 an) et qui est, dans la grande majorité des cas, secondaire à une exposition chronique aux fibres damiantes. Le mésothéliome est caractérisé par sa très grande latence de développement (3 à 5 décades après lexposition aux fibres toxiques). Il se développe préférentiellement dans le 1/3 inférieur de la plèvre et se manifeste initialement par un épaississement diffus de la plèvre.
b) Les endothéliums sont constitués de cellules endothéliales et forment le tissu de revêtement de la surface endoluminale des vaisseaux. A la différence des cellules épithéliales, les cellules endothéliales nexpriment pas la cytokératine, ne sont pas toujours réunies par des jonctions serrées et reposent sur un tissu conjonctif peu développé , nommé couche sous-endothéliale. Elles ne sont jamais réunies par des complexes de jonctions et peuvent même être non jointives. La diversité de structure des endothéliums est plus marquée pour les capillaires. Il existe trois types de capillaires.
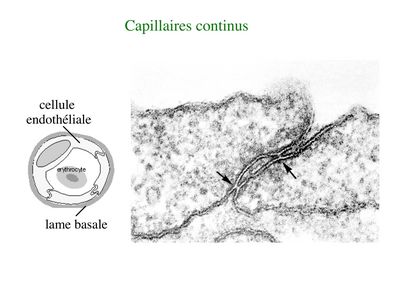
* Les capillaires continus sont les plus fréquents dans lorganisme. Les cellules endothéliales sont réunies par des jonctions serrées de type macula occludens (et non zonula occludens comme dans les épithéliums). Labsence de zonula occludens, laisse lespace paracellulaire partiellement ouvert au passage de molécules et de cellules. Cette caractéristique est particulièrement importante pour les fonctions dimmunosurveillance exercées par les globules blancs dans le tissu conjonctif des organes (on verra que le tissu conjonctif entoure et s'insinue dans les organes pleins et partcipe à la formation des muqueuses et de la peau). La lame basale est continue et se dédouble par endroit pour accueillir des péricytes (cellules musculaire lisse qui présentent des propriétés contractiles et de phagocytose).
* Les capillaires fenestrés sont caractérisés par la présence de pores trans-cytoplasmique au sein des cellules endothéliales. Ces pores facilitent le passage des molécules sanguines. La lame basale est en revanche continue. Les capillaires fenestrés sont présents dans les sites anatomiques ou les échanges moléculaires sont abondants et importants pour des fonctions de filtration (glomérule rénale, plexus choroïdes) ou d'absorption (villosité intestinales)(attention : ne pas confondre villosité intestinales et microvillosités des cellules épithéliales de l'intestin, les entérocytes).
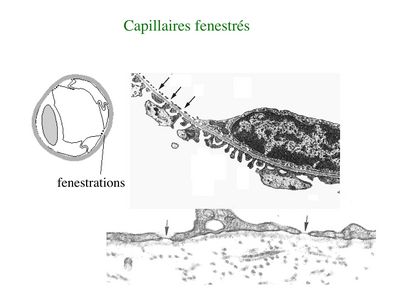
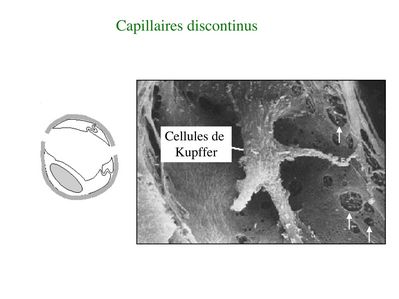
* Les capillaires discontinus sont formés de cellules endothéliales non jointives (interstices ente les cellules), présentant de larges pores trans-cytoplasmiques et reposant sur une lame basale discontinue. Cest le cas au niveau des capillaires du foie (capillaires sinusoïdes), de la rate (organe hématopïétique secondaire) et de la moelle osseuse (organe hématopoïétiques primaires). Dans la rate et la moelle osseuse, ces spécificités histologiques permettent le passage de cellules à travers la barrière endothéliale. Dans le foie, elles permettent lancrage intravasculaire des macrophages résidents du foie, les cellules de Kupffer.
c) Les épithéliums sensoriels sont constitués de neurones sensoriels et de cellules gliales de soutien. Ils sont apparentés aux tissus épithéliaux de revêtement car ils forment une couche de cellules jointives reposant sur une lame basale.
C) Classification :
Elle est basée sur 3 critères principaux : le nombre de couches cellulaires, la forme des cellules et leur état de différenciation.
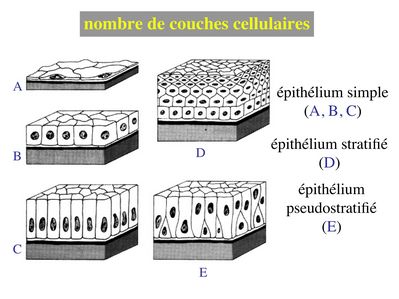
1) nombre de couches cellulaires : selon le nombre de couches cellulaires on parlera d'épithélium simple ou dépithélium stratifié (synonyme = pluristratifié ; bistratifié lorsquil y 2 couches). Un cas particulier, les épithéliums pseudostratifiés : en microscopie optique on observe un étagement des noyaux et des corps cellulaires donnant limpression dun stratification. En microscopie électronique, on observe toutefois que toute les cellules sont en contact avec la lame basale (on est donc plus proche dun épithélium simple au sens strict du terme).
2) forme des cellules : on parle d'épithélium pavimenteux lorsque les cellules sont plus larges que hautes, d'épithélium cubique lorsque les cellules sont aussi larges que hautes et d'épithélium cylindrique ou prismatique lorsque les cellules sont plus hautes que larges. Lorsqu'il s'agit d'épithéliums stratifiés, on ne prend en compte que la couche cellulaire superficielle pour décrire lépithélium. De la même façon, on définit les épithéliums pseudostratifiés en fonction de la couche cellulaire qui, en apparence, est la plus superficielle.
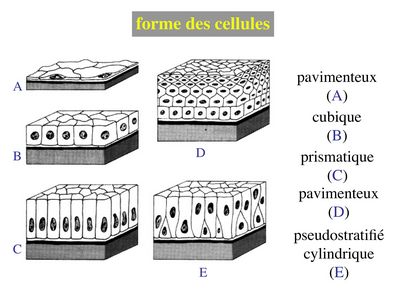
La combinaison des 2 critères (forme et nombre de couches) permet de discerner 5 principales catégories d'épithéliums : pavimenteux simple, cubique simple, cylindrique simple, pavimenteux pluristratifié, pseudostratifié.
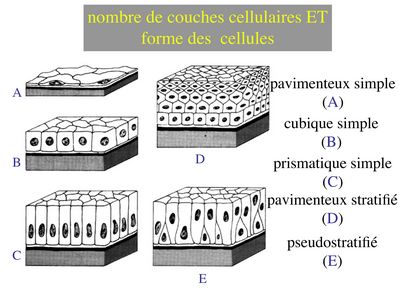
Enfin, il faut noter que les épithéliums pluristratifiés pavimenteux peuvent être nommés épithéliums malpighiens, du nom de celui qui les a décrits (Malpighi).
3) état de différenciation cellulaire : les différenciations les plus fréquentes sont les différenciations dites apicales. Elles concernent principalement le domaine apical de la membrane plasmique. Plus rarement, on observe dans les épithéliums de revêtement une différenciation du pôle apical (i.e de la portion apicale du cytoplasme). Par ailleurs, les cellules de lépiderme sont le siège dune différenciation spécifique, concernant lensemble du cytoplasme et qui est nommée kératinisation.
3-1 différenciations du domaine apical de la membrane plasmique: Il s'agit dexpansions du domaine apical de la membrane plasmique revêtant 3 formes : les microvillosités, les cils vibratiles et les stéréocils.
a) les microvillosités sont des expansions en doigt de gant qui peuvent être isolées ou au contraire très nombreuses (jusquà plusieurs milliers par cellules) et qui peuvent sorganiser alors en rangées ordonnées. On parle dans ce cas de plateau strié ou de bordure en brosse (termes synonymes). Les deux localisations les plus typiques de la différenciation en plateau strié sont lépithélium intestinal et lépithélium du tube contourné proximal du rein. Les microvillosités sont recouvertes dun revêtement glycoprotéique riche en enzymes : le cell coat ou glycocalyx. Lorsque les microvillosités sont très nombreuses, en particulier lorsqu'elles forment une bordure en brosse, le glycocalyx est visualisable en microscopie optique par la réaction de Schiff à lacide périodique (PAS).
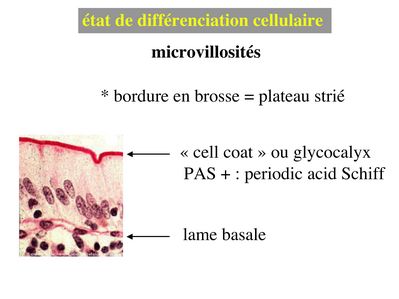
Le PAS colore en rouge les résidus glycosylés présents au niveau du cell coat, de la lame basale et au niveau des sécrétions muqueuses d'une façon générale. Lultrastructure des microvillosités comprend un axe central de quelques dizaines de microfilaments dactine qui sancrent à un réseau de microfilament localisé sous le domaine apical de la membrane plasmique : le plateau terminal (ou terminal web). Au plan moléculaire, les microfilaments dactine sassocient à un ensemble de molécules qui permettent de maintenir la structure des microvillosités lors de leurs mouvements passifs ou actifs. Les mouvements actifs permettent en particulier le retour en position "repos" des microvillosités.
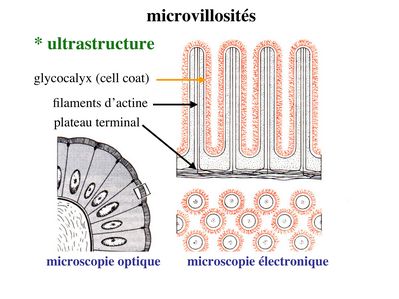
Pour mémoire :i) la villine et la fimbrine permettent la fasciculation (i.e lassemblage en faiceaux) des microfilaments d'actine
ii) la myosine 1 et l'ézrine permettent lattachement des microfilaments dactine à la membrane plasmique
iii) la spectrine assure les interconnexions entre filaments dactine au niveau du plateau terminal. La fonction des microvillosités est double : augmenter la surface de défense (image montrant une bactérie s'attachant aux microvillosités intestinales) et augmenter la surface déchange et dabsorption.
b) les cils vibratiles : il sagit dexpansions cytoplasmiques mobiles et dont les battements sont synchrones (les microvillosités sont mobiles mais nont pas de mouvements synchrones). Les cils vibratiles permettent le déplacement de sécrétions muqueuses. Les exemples les plus typiques sont donnés par lépithélium bronchique et lépithélium des trompes utérines (oviducte).
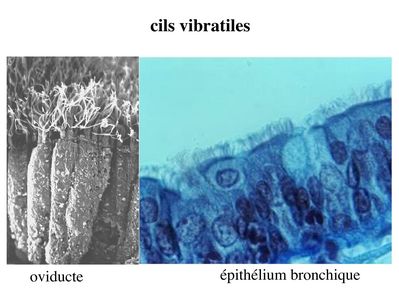
En microscopie optique, les cils vibratiles sont détectables en coloration standard du fait de leur longueur (10 fois plus long que les microvillosités) et de la présence d'une ligne localisée sous le domaine apical de la membrane plasmique, la ligne des corpuscules basaux.
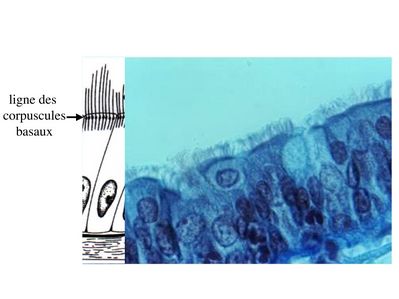
Les cils vibratiles sont formés schématiquement d'un axe contenant des éléments du cytosquelette, l'axonème, et d'une racine ciliaire qui est séparée de l'axonème par deux structures qui sont le corpuscule basal et la plaque basale.
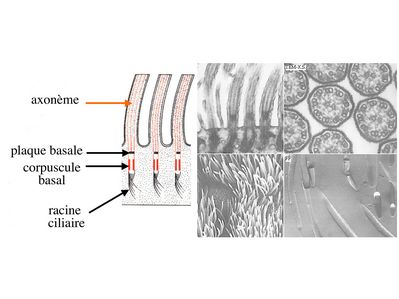
À la différence des microvillosités qui sont formés de microfilaments, l'axe des cils i.e l'axonème est constitué de microtubules qui suivent une organisation spatiale extrêmement précise. Cette structure microtubulaire est commune aux cils vibratiles et aux flagelles des spermatozoïdes.
Pour mémoire :
On y trouve 4 types de microtubules : les MT dit de type A et B forment 9 doublets périphériques et les microtubules C1 et C2 forment des singletons centraux. Ces deux singletons sont entourés d'une fine membrane, la membrane centrale, qui est reliée aux doublets périphériques par les fibres rayonnantes encore appelées radial spokes. Les doublets de microtubules sont reliés entre eux par des molécules de nexine et envoient ce qu'on appelle des bras internes et externes de molécules de dynéine qui portent l'activité ATPasique indispensable au battement ciliaire. C'est le mouvement synchronisé des molécules de dynéine davant en arrière qui va entraîner la flexion de l'axonème. L'association en doublet des microtubules de type A et B s'effectue par la mise en commun de protofilaments de tubuline (un protofilament est issu de la polymérisation d'une multitude de molécules de tubuline alpha et beta). Seul le microtubule A possède 13 protofilaments alors que le microtubule B n'en possède que 10 et forme un cercle incomplet accolé au microtubule A.
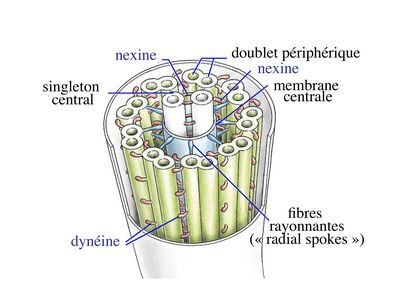
Par ailleurs, les microtubules de l'axonème sont en permanence renouvelés et organisés à partir d'une structure de type centriole, localisée sous le domaine apical de la membrane plasmique : le corpuscule basal. Dans cette zone, l'alignement des corpuscules basaux forme une ligne visible en microcopie optique : la ligne des corpuscules basaux. Comme les centrioles, les corpuscules basaux ne présentent pas de microtubules centraux et sont formés de triplets de microtubules périphériques au nombre de 9. Le corpuscule basal est relié d'une part à l'axonème par une structure nommée plaque basale et d'autre part au cytoplasme sous-jacent par la racine ciliaire (structure fibreuse dont la composition et les fonctions sont mal définies).
c) stéréocils : (stéréocils signifie "qui mime les cils"). Les stéréocils se présentent comme des expansions fines, irrégulières et parfois anastomosés de la membrane plasmique. Ils ne sont pas doués d'activité motrice. À la différence des cils, les stéréocils ne sont pas constitués de microtubules et ne comprennent pas de corpuscules basaux. Un exemple typique est donné par le canal de l'épididyme.
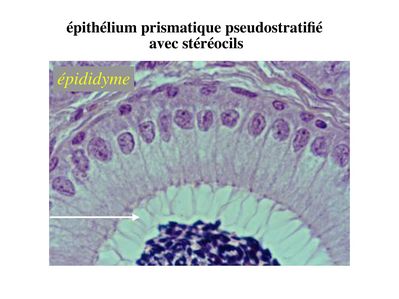
3-2 différenciations du pôle apical : La présence de mucus dans le cytoplasme apical de cellules épithéliales de revêtement définit une sous-population possédant une double appartenance aux tissus épithéliaux de revêtement et glandulaire.
Ces cellules prennent deux aspects distincts en microscopie optique :
a) les cellules dites à pôle muqueux ouvert : dans ces cellules, l'importance des phénomènes d'exocytose donne l'impression, en microscopie optique, d'une absence de membrane plasmique apicale (bien entendu, en microscopie électronique, on peut observer le domaine apicale de la membrane plasmique). Ces cellules sont nommées cellules caliciformes. L'exemple typique est celui des cellules caliciforme de l'épithélium intestinal. Ces cellules caliciformes s'insinuent entre les cellules épithéliales spécifiques de l'intestion, les entérocytes, et sont colorées par le PAS car elles contiennent un mucus riche en résidus glycosylés).
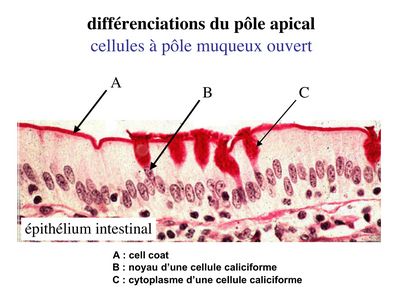
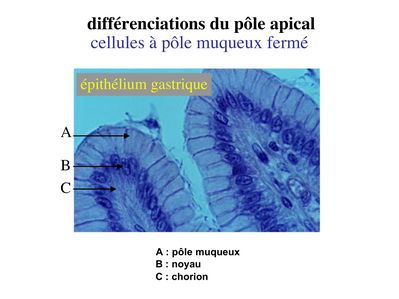
b) les cellules à pôle muqueux fermé : dans ces cellules, lexocytose du produit de sécrétion se est moins abontante et rapide que dans les cellules à pôle muqueux ouvert. On peu donc observer le domaine apical en microscopie optique. Le meilleur exemple est donné par les cellules de l'épithélium gastrique.
3-3 kératinisation : il s'agit d'une différenciation concernant l'ensemble de la cellule et qui est spécifique de l'épiderme (ne pas confondre kératinisation et expression de cytokératine). Lépiderme peut être défini comme un épithélium pavimenteux stratifié, kératinisé et dont les cellules épithéliales sont nommées kératinocytes. Le degré de kératinisation est inhomogène dune couche à lautre de lépiderme. Au cours de leur maturation, les kératinocytes migrent de la profondeur vers la superficie de lépiderme et sont soumis à un lent processus de kératinisation. La kératinisation consiste en l'accumulation intracytoplasmique de grains de kératohyaline puis de sacs de kératohyaline qui vont progressivement occuper l'ensemble de la cellule. Ainsi, l'épiderme est ainsi formé de 4 couches cellulaires qui correspondent à des degré de maturation et de kératinisation distincts.
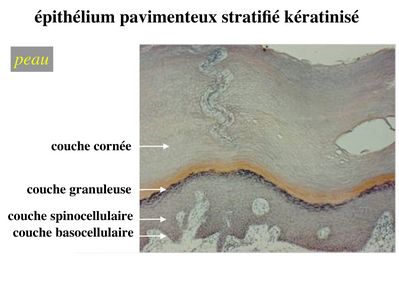
* la couche basocellulaire ou couche basale est au contact de la lame basale et est formé des cellules les plus immatures. On parle également de couche germinative. Elle est constituée d'une assise unique (monocouche) de cellules souches épithéliales reposant sur la lame basale. Ces cellules permettent le renouvellement permanent de lensemble des cellules épidermiques. En revanche elles ne sont pas capables de générer des structures annexes de la peau comme les poils, les glandes sébacées ou les glandes sudoripares.
* la couche spinocellulaire, localisée juste au dessus de la couche basale, est formée de plusieurs assises de cellules dont les membranes plasmiques sont reliées par de nombreux desmosomes. Labondance de desmosomes produit un aspect épineux en microscopie optique, doù le nom de couche spinocellulaire. Les cellules de cette couche sont le siège de nombreuses mitoses.
* la couche granuleuse est formée par 3 à 5 assises de cellules qui contiennent des grains de kératohyaline. La couche granuleuse marque le début du priocessus de kératinisation. Les cellules ny prolifèrent pas et présentent un petit noyau. On parle de noyau pycnotique.
* la couche cornée formée de cellules aplaties et anucléées renfermant des sacs de kératohyaline qui occupent l'ensemble du cytoplasme.
D) populations cellulaires spécifiques :
On trouve au sein des tissus épithéliaux de revêtement des cellules souches épithéliales et des cellules non épithéliales qui participent à des fonctions spécifiques au sein de chaque tissu épithélial.
1) cellules souches : après les cellules sanguines, les cellules épithéliales de revêtement sont les cellules de l'organisme présentant le renouvellement le plus rapide. Celui-ci est assuré par une population de cellules souches résidentes qui sont caractérisées par : i) leur grand potentiel de prolifération et ii) leur capacité à se différencier vers les types cellulaires épithéliaux du tissu dans lesquelles elles résident. Dans les épithéliums de revêtement, les cellules souches épithéliales peuvent prendre la forme dune assise de cellules basales participant à un épithélium stratifié. Cest le cas de la couche basale de lépiderme. Dans dautres cas, les cellules souches épithéliales sont isolées au sein du tissu épithélial et sintercalent entre cellules épithéliales matures. Elles sont néanmoins toujours en contact ou a proximité immédiate de la lame basale. Enfin, parfois les cellules souches se regroupent au sein de zones germinatives à partir desquelles les cellules filles migrent et renouvellent des régions de l'épithélium situées à distance de la zone germinative (ex : épithélium intestinal). Quelque soit le mode dorganisation des cellules souches épithéliales, (cellules isolées, assise basale et zone germinative), elles entretiennent des interactions étroites avec la lame basale. Ces interactions permettent le contrôle de la prolifération et de la différenciation des cellules souches. Dune façon générale on observe que toute cellule souche dans un tissu adulte, présente un micro-environnement spécifique qui va former ce quon appelle une niche pour la cellule souche. Le concept de niche permet de comprendre comment des signaux moléculaires délivrés par le micro-environnement contrôlent et éventuellement altèrent la fonction des cellules souches. Par exemple lors des processus de cancérisation, on considère actuellement que le micro-environnement des cellules souches pourrait altérer leur fonctionnement et conduire à la génération de cellules souches tumorales. Les cellules filles de ces cellules souches tumorales formeraient lensemble de la masse tumorale et présenterait des propriétés distinctes des cellules souches tumorales. : activité mitotique, rapport aux vaisseaux, suceptibilité à l'hypoxie, capacités d'efflux des molécules thérapeutiques. Alternativement, dautres hypothèses suggèrent que les cellules souches tumorales dérivent soit de cellules matures qui se sont dédifférenciées soit de cellules souches qui sont intrinsèquement tumorales (de façon indépendant de leur microenvironnement). Les implications thérapeutiques du concept de niche et de cellules souches tumorales sont très importantes.
2) cellules non épithéliales au sein des épithéliums de revêtement : nous prendrons comme modèle d'étude l'épiderme et les 3 types cellulaires non épithéliaux qu'il accueille: les mélanocytes, les cellules de Langerhans et les cellules de Merckel.
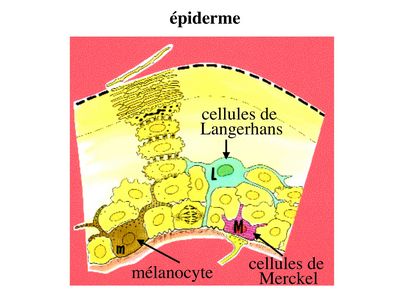
a) les mélanocytes : il s'agit de cellules à morphologie ramifiée, dérivant de la crête neurale, et dont la plus forte densité est trouvée à proximité de la lame basale. Elles contiennent des filaments intermédiaires de vimentine et non de cytokératine. Les mélanocytes sont responsables de la synthèse de mélanine, qui est essentiellement stimulée par lexposition aux rayons UV. Cette synthèse est réalisée au sein dorganites spécifiques, les mélanosomes. (organites : composants intra-cellulaires présentant une membrane propre les séparant du reste du cytoplame). Les mélanosomes migrent le long des prolongements cellulaires ramifiés des mélanocytes. Les mélanosomes sont ensuite captés par les kératinocytes et la mélanine y est stockée sous forme de grains de mélanine dans les lysosomes du kératinocyte. Chaque mélanocyte approvisionne ainsi plus de trente kératinocytes voisins, l'ensemble formant ce quon appelle une unité épidermique de mélanogénèse. La mélanine participe à la protection de l'épiderme contre les radiations UV. Une exposition inapropriée aux rayons UV peut conduire à la dégénérescence maligne des mélanocytes, à lorigine des mélanomes malins (pathologie tumorale cutanée à mauvais pronostic). En dehors de lépiderme, on trouve également des mélanocytes, en faible nombre, au niveau des muqueuses ainsi qu'au niveau de la rétine et des méninges.
b) les cellules de Langerhans : ce sont des cellules du système immunitaire localisées dans l'épiderme. Elles appartiennent à la famille des cellules dendritiques dont la principale fonction est la capture dantigènes et leur présentation aux lymphocytes T. En situation inflammatoire (secondaire à un traumatisme, une infection ou une tumeur par exemple), les cellules de Langerhans chargées d'antigènes (antigènes tumoraux par exemple) sont capables de migrer à travers la lame basale et de gagner les vaisseaux lymphatiques du tissu conjonctif sous-jacent. La circulation lymphatique leur permet de rejoindre les ganglions lymphatiques qui drainent le territoire cutané dont elles proviennent (par exemple ganglions axillaires pour une lésion du membre supérieur). Dans les ganglions lymphatiques, elles interagissent avec les lymphocytes T qui reconnaissent lantigène quelles présentent (on considère dune cellule dendritique est capable de « scanner » 10 000 lymphocyte T, à la recherche du lymphocyte T ad hoc). Cette interaction conduit à lactivation lymphocytaire cest-à-dire sa prolifération et lacquisition de propriétés migratoires spécifiques qui vont permettre son « homing » vers la zone epidermique inflammatoire.
c) les cellules de Merckel : ce sont des cellules à double valence épithéliale et neuroendocrine. Elles sont caractérisées par lexpression de cytokératine et par la présence abondante de granulations qui sont riches en neuropeptides. Les cellules de Merckel sont exclusivement localisées dans lépiderme des mains et des pieds au niveau des faces palmaire et plantaires. On considère quelles exercent essentiellement des fonctions de récepteurs sensitifs via des synapses établies avec des terminaisons nerveuses sensitives.
![]()