Eléments danatomopathologie des tissus épithéliaux.
A) Tumeurs épithéliales :
1) Généralités : les tumeurs épithéliales sont très fréquentes. Selon le type de cellule épithéliale dont elles dérivent, ces tumeurs présentent des caractéristiques anatomopathologiques distinctes. Il existe 3 grandes catégories de tumeurs épithéliales : les adénocarcinomes, les cancers épithéliaux de lépiderme et les cancers épithéliaux des muqueuses. Les adénocarcinomes dérivent de cellules épithéliales glandulaires et ont pour localisations les plus fréquentes la glande mammaire, la prostate et le tube digestif. Au sein du tube digestif, ladénocarcinome gastrique et ladénocarcinome pancréatique sont les plus fréquents. Les cancers épithéliaux de lépiderme, anciennement regroupés sous le terme dépithélioma, se subdivisent en 2 familles: les carcinomes spinocellulaires et les carcinomes baso-cellulaires. Enfin, les cancers épithéliaux développés au dépend dépithélium muqueux sont nommés carcinomes épidermoïdes. Les tumeurs épithéliales sont à distinguer des tumeurs développées au dépend de cellules non épithéliales résidant dans les épithéliums. Au niveau de lépiderme, il sagit du mélanome, du carcinome à cellules de Merckel et de lhistiocytose X (prolifération tumorale des cellules de Langerhans).
2) un exemple de carcinome cutané : le carcinome spinocellulaire.
Il sagit dune tumeur fréquente, après 50-60 ans sur les zones cutanées exposées de manière chronique au soleil. Cette tumeur se développe le plus souvent à partir de lésions cutanées pré-existantes tel que des cicatrices de brûlures ou des lésions de kératose sénile. Les localisations les plus fréquentes sont le cuir chevelu, le visage, les mains, les oreilles et la lèvre inférieure. Cette tumeur est formée de petits lobules intra-dermiques présentant une structure de type épiderme.
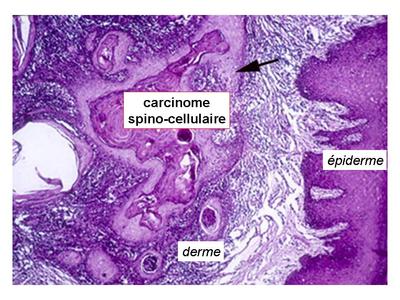
De la périphérie vers le centre de chaque lobule, on observe une assise de cellules analogues à la couche basale épidermique puis plusieurs assises de cellules polyédriques unies par des desmosomes et donc analogue à la couche spinocellulaire. Dans les formes les plus différenciées on observe une kératinisation centrale avec ou sans persistance des noyaux.
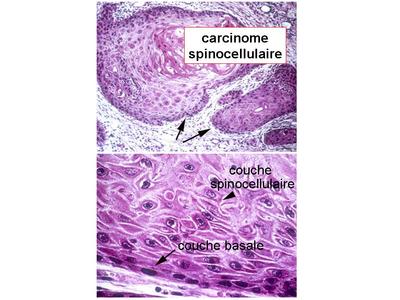
Les carcinomes spinocellulaires ont la capacité de métastaser à distance de leur site de localisation par voie sanguine ou lymphatique. Les métastases ganglionnaires, pulmonaires ou hépatiques sont les plus fréquentes. Par opposition au carcinome spinocellulaire, le carcinome basocellulaire correspond à une prolifération tumorale intra-épidermique de cellules de la couche basale. Il reste localisé et se développe le plus souvent à partir dune zone de peau saine.
3) un exemple dadénocarcinome : ladénocarcinome pancréatique
Dans la catégorie des adénocarcinomes, l'adénocarcinome pancréatique est une pathologie particulièrement redoutable. Il sagit d'un cancer qui survient le plus souvent chez lhomme entre 40 et 80 ans et qui débute au plan clinique par des douleurs abdominales suivi dun ictère ("jaunisse" liée à lenvahissement des voies biliaires). On observe une altération de létat général (Asthénie, Anorexie, Amaigrissement). Les tumeurs sont opérables dans seulement 15% des cas. La médiane de survie pour les cas inopérables est de 6 mois (soit 50% survivants 6 mois après diagnostic).
Au plan anatomopathologique, on observe la présence de structures canalaires de type canal excréteur, au sein du parenchyme glandulaire.
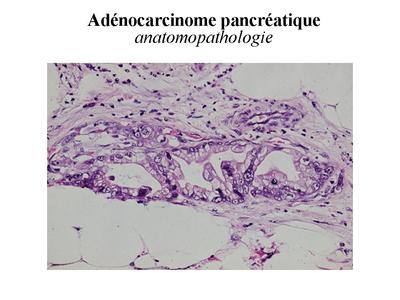
Ces structures infiltrent le tissu pancréatique dans son ensemble, y compris les terminaisons nerveuses sensitives (dou les douleurs souvent intenses).
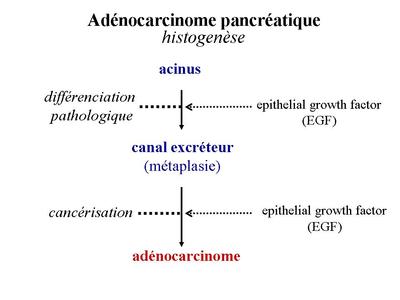
On considère actuellement que lhistogénèse de ladénocarcinome pancréatique débute par la différenciation dacinus en structures canalaires de type canal excréteur. Ces lésions précancéreuses sont dites métaplasiques. Dun façon générale, le terme de métaplasie, désigne la localisation anormale dun tissu par ailleurs d'aspect normal. La métaplasie ne doit pas être confondue avec la dysplasie, terme qui désigne la présence dun tissu anormal mais nayant pas encore les caractéristiques dun tissu cancéreux. Dans le pancréas, la cancérisation des métaplasies canalaires survinet dans un deuxième temps et est lié à un défaut de contrôle de la prolifération cellulaire. Des travaux récents ont montré que ces 2 phases de l'histogenèse des adénocarcinomes pancréatiques (métaplasie puis cancérisation) sont en partie liés à l'action d'une molécule : lEGF ("epithelial growth factor"). Implication thérapeutique : un inhibiteur du récepteur à l'EGF a été développé et a montré une efficacité supérieure aux traitements de référence pour l'adénocarcinome pancréatique.
Autres exemples dadénocarcinome, ladénocarcinome mammaire et ladénomarcinome prostatique présentent des similitudes physiopathologiques : dépendance hormonale (hormono-dépendance plus fréquente pour le cancer de la prostate), susceptibilité génétique (bien identifiée pour le cancer du sein : gènes BRCA pour BReast CAncer ; non identifiée pour le cancer de la prostate), extension lymphatique fréquente extension sanguine fréquente (métastases : foie, poumons, os, cerveau)
4) un cas particulier : le cancer intra-épithélial (cancer in situ) : ce terme désigne les tumeurs épithéliales (de revêtement ou glandulaire) qui ont un potentiel d'extension extra-épithélial mais qui se présentent à un stade évolutif ou leur localisation reste strictement intra-épithéliale, donc sans franchissement de la lame basale.
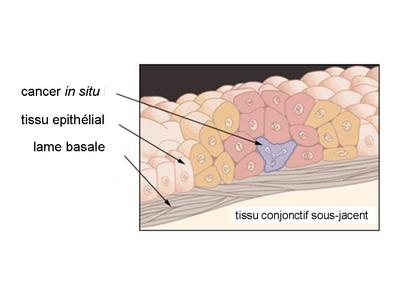
Lexemple le plus fréquent est le carcinome in situ de la muqueuse du col utérin. En labsence de traitement, lévolution naturelle est un envahissement de la lame basale et le développement de métastases. Dans ce processus métastatique on considère que les cellules cancéreuses envoient des signaux pro-inflammatoires aux fibroblastes du chorion qui, en retour, vont synthétiser des métalloprotéases. Les métalloprotéases modifient la composition de la lame basale épithéliale et permettent la migration des cellules cancéreuses dans le chorion puis dans la lymphe et/ou le sang à travers la paroi des vaisseaux.
B) brûlures de la peau :
Les brûlures les plus fréquentes sont thermiques mais elles peuvent être également d'origine électrique ou chimique. Il existe 3 degrés de brûlures.
Les brûlures du premier degré
entraînent une rougeur et un dème superficiels avec prurit (démangeaisons et grattage). Il sagit dune atteinte isolée de la couche cornée de l'épiderme avec vasodilatation des vaisseaux sanguins du derme. La guérison est rapide après desquamation (exemple : le coup de soleil superficiel).
Dans les brûlures du deuxième degré, on distingue 2 stades de gravité différente :
- le stade superficiel, est caractérisé par une destruction de lépiderme dans son ensemble, à lexception de la couche basale. On observe la formation dune bulle qui se résorbe et cicatrise sans séquelles. Ces brûlures sont très douloureuses.
- le stade profond est caractérisé par la destruction partielle ou totale de la couche basale et de la partie la plus superficielle du derme. La destruction dune partie des filets nerveux du derme explique le caractère initialement peu douloureux de ces brûlures. Une cicatrisation spontanée reste possible lorsque persistent des îlots de cellules basales. Ces îlots permettent une repopulation cellulaire centrifuge et/ou centripète. Dans les autres cas une greffe est le plus souvent nécessaire.
- Dans les brûlures du troisième degré, on observe une destruction totale de l'épiderme et du derme, et labsence totale de sensibilité cutanée résiduelle. Labsence de douleurs au stade initial est suivi dans les 24-48h par la survenue de douleurs intenses liées notamment à la compression de terminaisons nerveuses sous-jacentes par les tissus nécrosés et oedematiés. La cicatrisation spontanée est impossible et une greffe est indispensable.
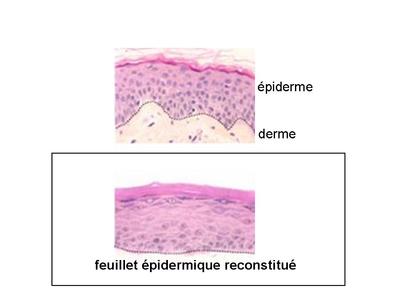
Pour les grands brûlés, les greffes de peau font actuellement appel à des techniques de thérapie cellulaire et dingénierie tissulaire. Ces techniques permettant de reconstituer en parallèle lépiderme et le derme. Pour ce qui concerne lépiderme, des prélèvements cutanés en zone saine sont réalisés afin disoler et de mettre en culture des cellules souches épithéliales. Après une quinzaine de jours de culture, ces cellules génèrent in vitro un feuillet épidermique complet qui sera greffé.
![]()